Material que necesitamos
-
3,3 g de nitrato de plomo II, Pb(NO3 )2 , disueltos en un litro de agua.
- 3,3 g de yoduro de potasio, Kl, disueltos en un litro de agua.
- Dos tubos de ensayo.
- Dos pipetas de 5 cm 3 .
- Un mechero de gas para calentar el tubo de ensayo, con las correspondientes pinzas.
Aplicación
didáctica
Si ponemos en contacto el yoduro de potasio, Kl, y el nitrato de plomo
II, Pb(NO3 )2 , se transforman en nitrato
de potasio, KNO3,
y yoduro de plomo II, Pbl2. Este proceso está descrito por
la ecuación:
2
Kl +Pb(NO3 )2 .2 KNO3 +Pbl2
La flecha hacia abajo indica que el producto no se disuelve en agua y
precipita. Este compuesto es amarillo y al precipitar parece una lluvia
dorada.
Para conseguirlo disuelve los 3,3 g de cada sal en un litro de agua, en
botellas separadas.
Toma, con pipetas distintas, 5 cm 3 de cada disolución y viértelos
en cada tubo de ensayo. Echa el contenido de un tubo en el otro. El aspecto
transparente de cada reactivo se convierte en amarillo turbio. Es el yoduro
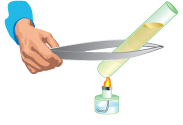
de plomo II que precipita. Calienta con cuidado el tubo de ensayo con
la llama del mechero, paseando el tubo por la llama con un movimiento
de vaivén.No sigas calentando cuando comience a hervir. En este momento
el aspecto se volverá casi transparente: como casi todos los sólidos,
el yoduro de plomo II se disuelve mejor en agua caliente que en agua fría.
Espera unos instantes y pon el tubo debajo del grifo del agua fría, con
cuidado de que no entre agua en el tubo. En pocos minutos se verán unas
pequeñas escamas doradas moviéndose en el agua. Es el yoduro de plomo
II de nuevo. ¡Parecen de oro!