![]()
ADN contra enfermedades, ¿podría el ADN acabar con el COVID-19?
Daniel Peñas Utrilla y Raúl Valero Carabias,
Biotecnología Clínica y Farmacéutica
La búsqueda de tratamientos que erradiquen determinadas enfermedades; una vez esta sea adquirida por el paciente, es uno de los objetivos principales que nos ocupa actualmente, puesto que todavía no se ha desarrollado completamente una vacuna preventiva frente al COVID-19. La purificación de anticuerpos de pacientes inmunizados frente al coronavirus es uno de los posibles tratamientos que se está aplicando actualmente (1), pero hay otra posible alternativa que presenta una serie de ventajas que posteriormente serán expuestas. Dicha alternativa son los aptámeros.
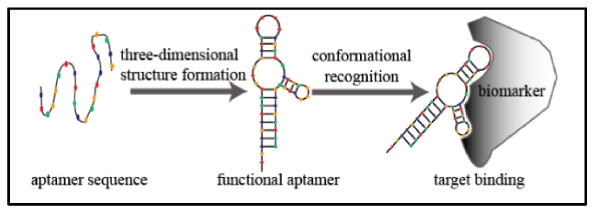
Los aptámeros se definen como una secuencia sencilla de oligonucleótidos de ADN o ARN, de corta longitud que reconoce moléculas diana. Gracias a ello puede adquirir una estructura que le permite unirse con facilidad a la molécula diana (Figura 1) (2).
Figura 1. Representación esquemática de la estructura y función de los aptámeros. Imagen obtenida de Sun and Zu, 2015 (4).
Se obtienen por un método conocido como SELEX (Systematic evolution of ligands by expontential enrichment), proceso que nació de la mano de Larry Gold alrededor del año 1990 con el objetivo de obtener oligonucleótidos de una sola cadena que se unan a moléculas diana con elevada especificidad y afinidad. Curiosamente, al mismo tiempo y de forma independiente, otros dos investigadores, Andy Ellington y Jack Szostak, consiguieron seleccionar ligandos basados en ARN frente a una serie de colorantes orgánicos. Precisamente, fue el laboratorio de Szostak el que acuñó el término de aptámero (del latín aptus, que significa “unir” o “fijar” y del griego meros, que significa “partícula”) (3).
Unos años más tarde, se descubrió la presencia de aptámeros existentes de forma natural en organismos vivos. Estas moléculas fueron bautizadas como riboswitches (ribointerruptor) y se tratan de un elemento presente en el extremo 5’ del ARN mensajero que es capaz de interaccionar con algunos metabolitos in vivo (5). Visto el origen y la definición de esta molécula, ¿qué ventajas supone frente a los anticuerpos? ¿Qué potencial posee para acabar sustituyendo a los mismos? Frente a su producción, no es dependiente de animales ni de células, sino que se realiza mediante síntesis química, por lo que el tiempo de producción se ve reducido. Además, el fenómeno de variabilidad de moléculas dentro del mismo lote, que ocurre en la producción animal o mediante cultivos celulares, disminuye significativamente.
Por otro lado, como no necesitan ambientes ligados a carácter fisiológico, se puede deducir que los aptámeros son moléculas con mayor estabilidad. Todo ello reduce los costes del proceso, ya sea frente a la purificación del lote resultante o el control de las condiciones del reactor, por lo que el precio del producto en el mercado se verá reducido, debido a que será más fácil encontrar su rentabilidad.
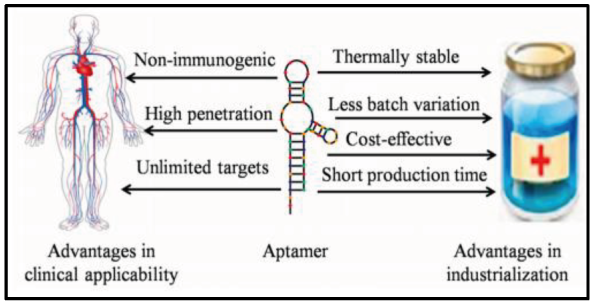
Con relación a la aplicación clínica, no poseen inmunogenicidad, evitándose así los posibles efectos secundarios relacionados con reacciones alérgicas. Al ser de menor tamaño, el acceso a cualquier tejido se encuentra facilitado. Así mismo, presentan propiedades de reconocimiento equiparables a las de los anticuerpos monoclonales o incluso mayores, siendo capaces de diferenciar cambios mínimos estructurales como ocurre en el caso de la teofilina y la cafeína, dos compuestos que se distinguen únicamente en un grupo metilo en su estructura (Figura 2) (4).
Figura 2. Ventajas de los aptámeros frente a los anticuerpos en el ámbito industrial y farmacéutico. Imagen obtenida de Sun and Zu, 2015 (4).
En la actualidad, los campos en los que se emplean los aptámeros incluyen diagnóstico clínico y análisis de alimentos; es decir, el uso de aptámeros como biosensores y terapia, investigación y biotecnología, en todos los casos debido a la especificidad de la interacción aptámero-diana. El diagnóstico clínico es un campo en el que se están realizando grandes progresos gracias al uso de la tecnología de los aptámeros, ya que, como se puede observar en los estudios llevados a cabo por Gold (6), se ha desarrollado un sensor proteómico basado en aptámeros capaz de medir simultáneamente más de 800 proteínas diferentes en una pequeña muestra de sangre (2).
En relación con la pandemia que está afectando a la mayor parte del mundo en estos momento, encontrar una forma de detectar la presencia del coronavirus y así poder identificar a las personas contagiadas, incluso siendo asintomáticas, es clave para poder hacerle frente. Este tipo de diagnóstico podría ser realizado mediante la tecnología de los aptámeros ya que, en 2011 fue identificada una molécula de aptámero de ADN de cadena sencilla (ssDNA) que podía unirse de forma específica a la proteína N de la nucleocápside del CoV SARS, virus responsable del SARS en 2002 (7). Este descubrimiento podría abrir una puerta hacia el uso de moléculas de aptámeros para dirigir tratamientos de forma específica hacia el COVID-19.
En la actualidad, el primer medicamento basado en la tecnología de los aptámeros, fue comercializado y aprobado por la FDA (Food and Drug Administration) en 2004, se trata del Pegaptanib, también conocido como Macugen. La diana de este aptámero es el factor de crecimiento endotelial vascular (VEGF), permitiendo el tratamiento de la degeneración macular asociada a la edad, al inhibir la neovascularización en el coroide, capa de vasos sanguíneos y tejido conectivo entre la parte blanca del ojo y la retina (8,9).
En la base de datos ClinicalTrials.gov asociada al U. S. National Library of Medicine se recopilan actualmente 43 estudios sobre la aplicación de aptámeros al tratamiento, encontrándose la mayoría en las primeras fases del desarrollo del medicamento. La mayor parte de estos estudios se encuentran enfocados a enfermedades oculares, tales como la anteriormente mencionada o la retinopatía diabética, aunque también se está aplicando en terapia contra el cáncer de mama, colorrectal y en enfermedades parasitarias, como la enfermedad de Chagas (10,11). Estos últimos estudios se encuentran en fase II.
Una de las empresas que dedica toda su investigación al desarrollo de esta tecnología es la compañía biofarmacéutica española AptaTargets. Fue fundada en Madrid en el año 2014 y ha conseguido patentar un aptámero con la capacidad de unirse específicamente a TLR-4, una proteína transmembrana que inicia una serie de cascadas de señalización que acaban activando al sistema inmunológico innato. Las aplicaciones de este aptámero van desde la detección del receptor TLR-4, pasando por su inhibición y llegando hasta dirigir un determinado fármaco a células que sobreexpresan este receptor, pudiendo ser empleado como inmunosupresor para todo tipo de trasplantes (12).
Toda esta información hace plantearnos una pregunta. Si los aptámeros son una tecnología tan eficaz frente a distintos aspectos del ámbito científico, ¿por qué no se está consiguiendo implantar en detrimento del uso de los anticuerpos monoclonales? ¿Es posible que no sea tan maravilloso como parece? Empezando en los primeros pasos del desarrollo de un determinado aptámero frente a una diana específica, se ha podido observar falta de rigor en relación con la reproducibilidad de los ensayos. Este problema también se da en la producción de anticuerpos monoclonales, pero es más notorio en esta molécula, debido al menor desarrollo de su tecnología (13).
El siguiente contratiempo se encuentra a nivel de producción industrial, ya que el método SELEX requiere pago de propiedad intelectual al encontrarse bajo patente, lo que impide el libre acceso a esta tecnología. Por último, la gran competitividad del mercado frente a su rival directo, los anticuerpos monoclonales, relevan la utilización de aptámeros a un segundo plano. Esto se puede ejemplificar con respecto al único producto de esta índole que se encuentra actualmente en el mercado, el Pegaptanib, siendo superado por su homólogo proteico, el Ranibizumab el cual ha demostrado tener mayor eficacia en el tratamiento de la degeneración macular asociada a la edad (9).
La estandarización del diseño de experimentos para la comprobación de la efectividad de los aptámeros en su salto de in vitro a in vivo determinará el futuro de esta molécula de gran potencial terapéutico y diagnóstico, gracias a la considerable especificidad respecto a su diana clínica.
Bibliografía
(1) Yu, Fei; Du, Lanying; Ojcius, David M.; Pan, Chungen and Jiang, Shibo. 2020. Measures for diagnosing and treating infections by a novel coronavirus responsible for a pneumonia outbreak originating in Wuhan, China. Microbes and Infection. 22 (2). 74-79. (2) Hernández, Frank J. and Botero Hincapié, Juliana Andrea. (2012). Aptámeros: agentes diagnósticos y terapéuticos. Iatreia. 25 (2). 159-168. (3) Ellington, A. and Szostak, J. (1990). In vitro selection of RNA molecules that bind specific ligands. Nature 346, 818–822.
(4) Sun, Hongguang and Zu, Youli. (2015). A Highlight of Recent Advances in Aptamer Technology and Its Application. Molecules. 20. 11959-11980. (5) Lee, Chang Ho; Han, Seung Ryul and Lee, Seong-Wook. (2016). Therapeutic Applications of Aptamer-Based Riboswitches. Nucleic Acid Therapeutics. 26 (1). (6) Gold, L.; Ayers, D.; Bertino, J.; Bock, C.; Bock, A.; Brody, E. N. et al. (2010). Aptamer-based multiplexed proteomic technology for biomarker discovery. PloS one. 5(12): e15004. (7) Cho, S.-J.; Woo, H.-M.; Kim, K.-S.; Oh, J.-W. and Jeong, Y.-J. (2011). Novel system for detecting SARS coronavirus nucleocapsid protein using an ssDNA aptamer. Journal of Bioscience and Bioengineering, 112(6), 535–540.
(8) U.S. National Library of Medicine. (1998). MedicinePlus®. Recuperado de https://medlineplus.gov/
(9) Stein, Cy A. and Castanotto, Daniela. (2017). FDA-Approved Oligonucleotide Therapies in 2017. Molecular Therapy. 25 (5). 1069-1075.
(10) U.S. National Library of Medicine. (2008). ClinicalTrials.gov. Recuperado de https://clinicaltrials.gov/ct2/home
(11) Ospina Vila, Juan David. (2020). Aptámeros como novedosa herramienta diagnóstica y terapéutica y su uso en parasitología. Biomédica. 40 (2). 1-46. (12) AptaTargets. (2014). Patents. Recuperado de http://aptatargets.com/about-us/patents
(13) Yan, Amy C. and Lewy Matthew. 2018. Aptamer-Mediated Delivery and Cell-Targeting Aptamers: Room for Improvement. Nucleic Acid Therapeutics. 28 (3). 194-199.