![]()
Células CAR-T aplicadas con éxito en la Comunidad de Madrid
.0Alfredo Rus
El pasado 9 de enero, la Consejería de Sanidad de la Comunidad de Madrid dio a conocer que se había tratado a 41 pacientes de cáncer hematológico empleando técnicas avanzadas de terapia génica y terapia celular, abundando el empleo de la tecnología de células CAR-T. Los centros responsables de estos tratamientos Unidad Infanto-juvenil del Hospital La Paz y el Servicio de Hematología del Hospital Gregorio Marañón, ambos coordinados por la Unidad de Terapias Avanzadas de la Comunidad de Madrid.
Los resultados de estos tratamientos parecen ser de lo más halagüeño, ya que de los 41 pacientes tratados hasta la fecha seis han alcanzado ya una remisión total. Si bien es aún pronto para evaluar con contundencia la eficacia de estos tratamientos, lo positivo de estos ensayos ha impulsado la financiación de nuevos ensayos con células CART-T en los hospitales 12 de octubre y Niño Jesús de Madrid a los que desde principios de este año 2020 se han añadido otros cinco: La Princesa, Ramón y Cajal, Clínico San Carlos, Puerta de Hierro y la Fundación Jiménez Díaz.
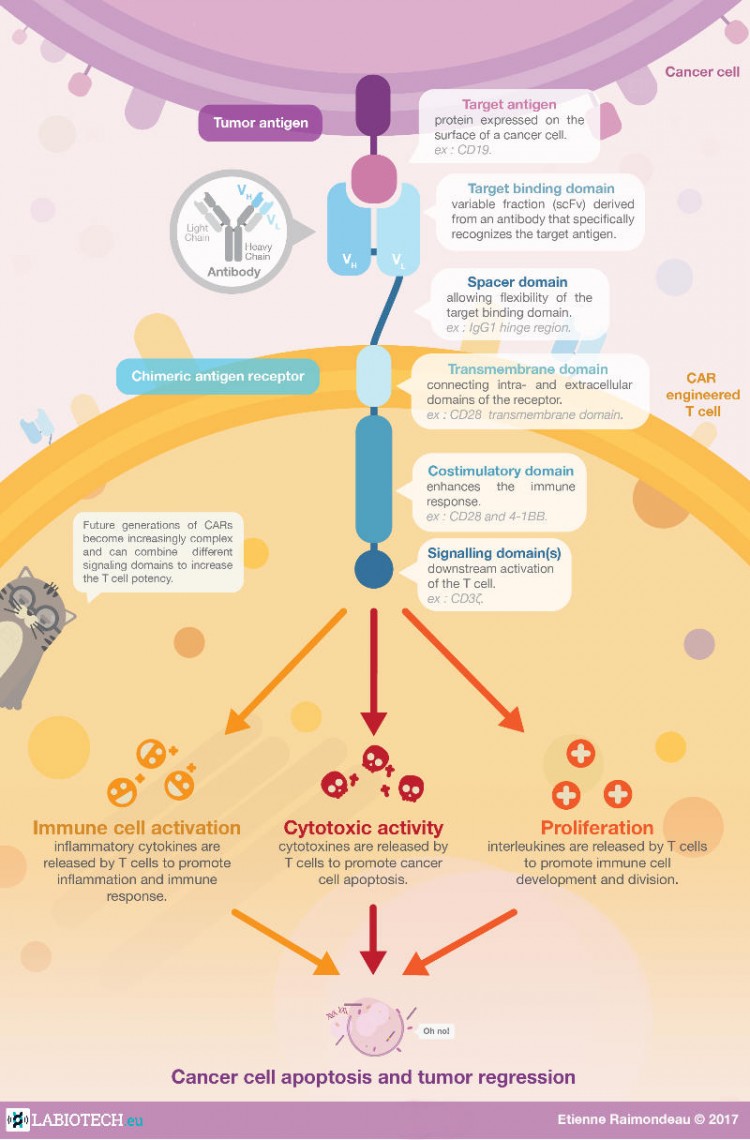
Pero, ¿en qué consiste exactamente el tratamiento con células CAR-T? Los medicamentos CAR-T se basan en la modificación genética de linfocitos T con el fin de hacerlos capaces de responder y atacar a células cancerosas. Su nombre, proviene de Chimeric Antigen Receptor, y resulta en sí mismo bastante revelador de su naturaleza. Los linfocitos T se extraen y aíslan de la sangre del propio paciente y, posteriormente, son modificadas genéticamente para que integren en su genoma un gen que codifica para este Receptor Antigénico Quimérico, el cual es diseñado por ingeniería genética y que confiere al linfocito la capacidad de reconocer al antígeno tumoral CD-19 (en el caso de las leucemias y linfomas como el de estos 41 pacientes, es la proteína CD-19 la que se expresa en la superficie de los linfocitos B alterados por el cáncer). Estas células pueden reconocer y eliminar células tumorales sin necesidad de la participación del TCR, teniendo el receptor CAR, en su parte citosólica, elementos que permiten que se produzca señalización sin necesidad de una coestimulación por CD80/CD86.
Los tratamientos con CAR-T se encuentran en la actualidad indicados para el tratamiento de leucemias linfoblásticas agudas (ALL), siendo 2 los tratamientos aprobados a día de hoy por la FDA.
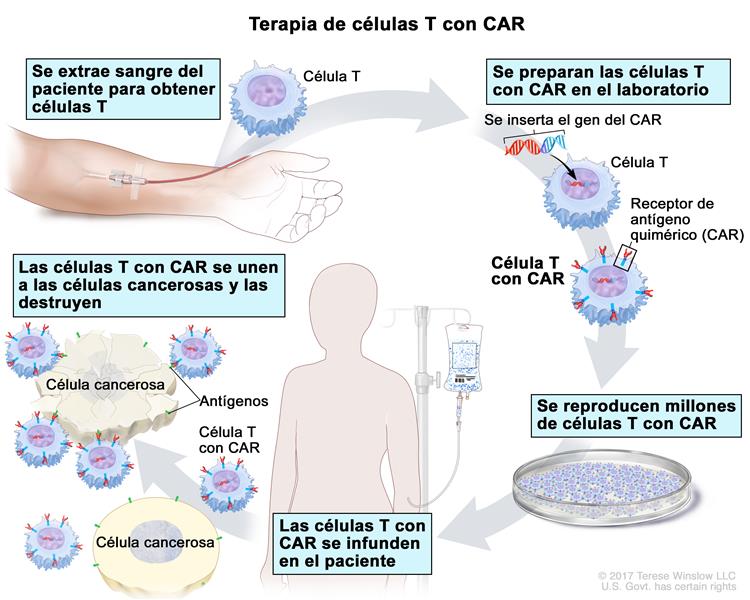
Salta a la vista, por tanto, que le tratamiento con Car-T es una combinación de terapia celular (ya que no se trata de un fármaco), inmunoterapia (puesto que son las propias células inmunes las que, en definitiva, atajaran el tumor) y de terapia génica (pues es indispensable la modificación genética de células inmunes y el diseño de todo un gen). Como tal, el tratamiento con CAR-T requieres de un total de ocho etapas bien diferenciadas:
– Aféresis: se extraen por leucaféresis los glóbulos blancos de la sangre del paciente, esto incluye, lógicamente, los linfocitos T.
– Reprogramación celular: se introduce un plásmido o vector retroviral en las células T que contiene el gen que codifica para el receptor CAR, permitiéndoles así reconocer las células cancerígenas junto con cualquier otra célula que exprese el antígeno específico a destruir.
– Expansión: se cultiva y multiplican las células T ya modificadas y son enviadas de vuelta al hospital.
– Preparación del paciente: se administra quimioterapia previa al paciente para prevenir un posible rechazo del organismo y asegurar así la proliferación en él de las células CAR-T. En definitiva, se pretende ayudar al cuerpo a que acepte las células reprogramadas.
– Infusión: se administran por vía intravenosa los linfocitos T modificados.
– Ataque de las células: si todo evoluciona correctamente, una vez en el torrente sanguíneo las células CAR-T cargan contra las células B y comienzan a destruirlas.
– Monitorización: en un 30-40% de los caso cabe la posibilidad de que se manifiesten efectos adversos, ya que estos linfocitos, son capaces de permanecer en el sistema inmune, con lo que se crea memoria inmunológica y pueden terminar reaccionando ante cualquier linfocito B, no solo los cancerosos.
– Seguimiento y resultados.
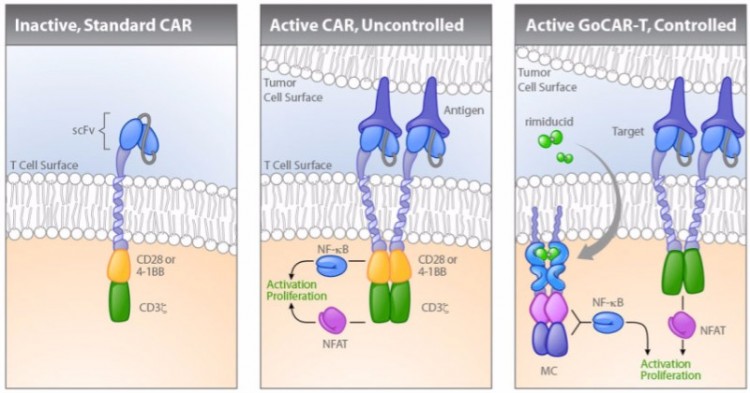
 Como se ha comentado, existe una posibilidad, nada desdeñable, de que aparezcan efectos secundarios por el tratamiento con CAR-T , siendo el más frecuente de ellos el síndrome de liberación de citoquinas, el cual se produce a consecuencia de la gran expansión que sufren las células CAR-T una vez han detectado su antígeno, expansión esta que a su vez provoca la liberación masiva de citoquinas a la sangre lo que puede resultar en síntomas que van desde una mera fiebre al fallo multiorgánico, si bien existen fármacos para mantener esta respuesta adversa bajo control. Otro efecto secundario destacable es la toxicidad neurológica que puede abarcar desde una cefalea a un derrame cerebral, aunque esta suele derivar del síndrome de liberación de citoquinas, por lo que el tratamiento de este suele resolver esta toxicidad neurológica. Para ambos hace frente a estos escenarios y a otros derivados de una actividad descontrolada de las células CAR-T se trabaja ahora en la tecnología GoCAR-T, que se sirve del fármaco Rimiduzid para activas las CAR-T a voluntad.
Como se ha comentado, existe una posibilidad, nada desdeñable, de que aparezcan efectos secundarios por el tratamiento con CAR-T , siendo el más frecuente de ellos el síndrome de liberación de citoquinas, el cual se produce a consecuencia de la gran expansión que sufren las células CAR-T una vez han detectado su antígeno, expansión esta que a su vez provoca la liberación masiva de citoquinas a la sangre lo que puede resultar en síntomas que van desde una mera fiebre al fallo multiorgánico, si bien existen fármacos para mantener esta respuesta adversa bajo control. Otro efecto secundario destacable es la toxicidad neurológica que puede abarcar desde una cefalea a un derrame cerebral, aunque esta suele derivar del síndrome de liberación de citoquinas, por lo que el tratamiento de este suele resolver esta toxicidad neurológica. Para ambos hace frente a estos escenarios y a otros derivados de una actividad descontrolada de las células CAR-T se trabaja ahora en la tecnología GoCAR-T, que se sirve del fármaco Rimiduzid para activas las CAR-T a voluntad.
 Si atendemos a las cifras, la tasa de respuesta al tratamiento para la ALL ronda el 90%, la de supervivencia a los dos años, el 80%; y los pacientes libres totalmente de enfermedad se aproximan a un 60%, según el Hospital Sant Joan Déu de Barcelona, uno de los centros europeos más implicados en la implementación de estas técnicas. Con todo, es importante recordar que las mayores tasas de éxito se corresponden con niños, adolescente y jóvenes menores de 25 años, por lo que aun se ha de ser prudente a la hora de juzgar la eficacia de la terapia CAR-T.
Si atendemos a las cifras, la tasa de respuesta al tratamiento para la ALL ronda el 90%, la de supervivencia a los dos años, el 80%; y los pacientes libres totalmente de enfermedad se aproximan a un 60%, según el Hospital Sant Joan Déu de Barcelona, uno de los centros europeos más implicados en la implementación de estas técnicas. Con todo, es importante recordar que las mayores tasas de éxito se corresponden con niños, adolescente y jóvenes menores de 25 años, por lo que aun se ha de ser prudente a la hora de juzgar la eficacia de la terapia CAR-T.
De cara al futuro, se mira con buenos ojos el desarrollo de la tecnología FasT CAR-T, que permitiría la producción rápida y a bajo coste de estas terapias para cánceres hematológicos, pasándose de los 30 días necesarios para la inyección en el paciente de las CAR-T a entorno a 10, en vista de que su manufacturación en el laboratorio es de tan solo 1 día. Además, los linfocitos anti-CD19 producidos por FasT CAR-T son más seguro y entre 20 y 40 veces más potentes que los usuales. Son todavía muchos los restos que aguardan a la tecnología CAR-T tanto para la ALL como para otras patologías pero son igualmente muchas las razones para mantener la esperanza en la lucha contra el cáncer basadas en estas técnicas.
Bibliografía:
– Comunidad de Madrid. Consejería de Salud. Acción de Gobierno. Noticias: https://www.comunidad.madrid/noticias/2020/01/09/hemos-tratado-41-pacientes-terapias-avanzadas-cancer
– Instituto Nacional del Cáncer (NIH): https://www.cancer.gov/espanol/publicaciones/diccionario/def/terapia-de-celulas-t-con-car
– Laboratorio Clinico Rafer. Terapia CAR-T, revolución en el abordaje del cáncer. Anabel Mainer | 2 Sep 2019 | Hematología: https://www.rafer.es/innovacion-laboratorio-clinico/terapia-car-t/
– Hospital Sant Joan de Déu (Barcelona). Inmunoterapia CAR-T 19.: https://www.sjdhospitalbarcelona.org/es/oncologia/inmunoterapia-cart19
– Labiotech.eu. “A Cure for Cancer? How CAR T-Cell Therapy is Revolutionizing Oncology”, Clara Rodríguez Fernández (10/09/2019).: https://www.labiotech.eu/car-t/car-t-therapy-cancer-review/