![]()
Nuevos recubrimientos sol-gel con liberación controlada de antifúngicos para prótesis articulares metálicas
El uso de implantes articulares conlleva, en la mayoría de los pacientes, a una mejora en su calidad de vida; aunque en ocasiones pueden generar consecuencias devastadoras para el paciente y para el Sistema de Sanidad Pública. A pesar de las medidas preventivas que se toman al implantar un biomaterial, es casi inevitable la presencia de microbios durante la intervención, que pueden desencadenar una infección. Estas infecciones asociadas a biomateriales (IAB) son tratadas usualmente con antifúngicos administrados por vía oral o parenteral, pero la concentración de los fármacos que alcanza la zona afectada es inferior a la detectada en sangre. Si se aumentase la dosis sistémica se correría el riesgo de provocar toxicidad orgánica; por lo que una alternativa para solventar dicha restricción sería administrar el fármaco de manera local.
![Figura 1 Etapas del proceso sol-gel [Modificado de B. Faure y colaboradores, 2013, Sci. Technol. Adv. Mater., vol. 14, no. 2] Figura 1 Etapas del proceso sol-gel [Modificado de B. Faure y colaboradores, 2013, Sci. Technol. Adv. Mater., vol. 14, no. 2]](https://www.madrimasd.org/blogs/tecnologia_polvos/files/2018/10/Figura-11-300x46.png)

Los recubrimientos se sintetizaron a partir de los precursores de silicio γ-metacriloxipropiltrimetoxisilano (MAPTMS) y tetrametoxisilano (TMOS) en una relación molar 1:2 con la introducción del antifúngico fluconazol a distintas concentraciones. En todos los casos se obtuvieron recubrimientos homogéneos (Figura 2). Además, todos los recubrimientos presentan similares espesores y grado de hidrofilicidad.
Los estudios electroquímicos realizados y la modelización de los valores de impedancia compleja mediante distintos circuitos equivalentes permitieron el estudio de los diferentes procesos físicos y/o químicos presentes en el sistema. Con la utilización de esta técnica se demostró que a mayor concentración de antifúngico, la velocidad de degradación del recubrimiento es mayor; aunque después de 24 horas de inmersión en el electrolito en todas las muestras aún existen zonas con recubrimiento. Un ejemplo de los diagramas de Nyquist obtenidos a partir de los ensayos realizados se muestra en la Figura 3. Este recubrimiento mostró el mejor comportamiento en cuanto a velocidad de degradación (durante 24 horas) y disminución del desarrollo del biofilm fúngico.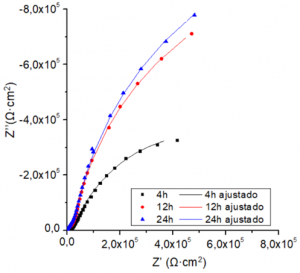
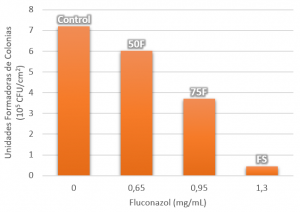
La acción farmacológica de los recubrimientos fue obtenida a partir de ensayos realizados en colaboración con el Departamento de Microbiología del Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz (IIS-FJD); donde se evaluó la disminución del desarrollo del biofilm. Los resultados de estos ensayos (Figura 4) demuestran que el principio activo del fármaco no se ve afectado por los procesos de síntesis y secado, ya que a mayor concentración de fluconazol disminuye en mayor medida el desarrollo del biofilm sobre el recubrimiento.