![]()
Preparación cromoselectiva de aminas, alcoholes y heterociclos Z- o E-alilados a través de una reacción de alilación fotocatalítica
Autor: José Julián Alemán Lara. UAM
En 1957 se publicó una fotografía en The New York Magazine donde podía verse a un hombre con los ojos vendados mezclando algunos reactivos y cuyo pie de foto decía: “El Dr Arnold Moore llevando a cabo un experimento para probar la teoría de que los mayores descubrimientos científicos se encuentran por accidente”. Este tipo de descubrimientos están basados en lo que se conoce como “Serendipia”.
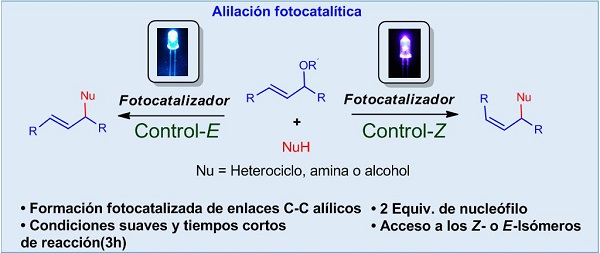
Durante la última década, el uso de la fotocatálisis ha abierto la puerta al desarrollo de nuevos métodos sintéticos que dan acceso a una amplia gama de moléculas activas, generalmente radicales, que siguiendo distintas vías dan acceso a productos de gran valor farmacológico y agrícola. Un ejemplo de ello es la reacción de arilación fotocatalítica, descrita por primera vez hace cinco años. Sin embargo, la version fotocatalítica de la reacción de alilación era desconocida hasta ahora. Trabajando con sistemas alílicos y fotocatálisis, Ana Martínez-Gualda, primera autora del proyecto que se describe a continuación, observó la formación de un subproducto que correspondía con la ruptura de un enlace C-O de un sistema alílico. Tras estudiar este resultado inespor: José Julián Aleman Laraerado se dio cuenta de que la importancia de esta transformación, lo que resulta un caso claro de serendipia. Dos años después, presentamos por vez primera la version fotocatalítica de la reacción de alilación de nucleófilos como heteroarenos, aminas y alcoholes (Figura 1). Esta nueva metodología permite la síntesis cromoselectiva de los compuestos Z– y E– alilados. Mientras que el uso de radiación UV permite obtener los hasta ahora inaccesibles compuestos Z-alilados, los isómeros E– pueden obtenerse mediante irradiación con luz visible y cambiando el sistema catalítico.
Fig. 1 Síntesis cromoselectiva fotocatalizada de compuestos alilados Z- o E– presentada en este trabajo.
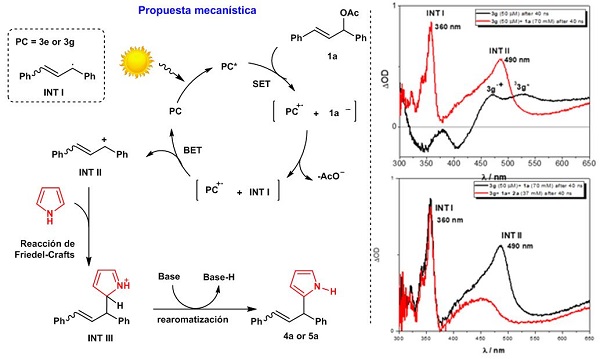
Uno de los aspectos más excitantes de este proyecto fue la elucidación del mecanismo de reacción mediante el trabajo de un excepcional grupo de investigadores que combinaron cálculos DFT, estudios de fotólisis de destello de láser y datos espectroscópicos (Figura 2). La detección de la formación de un carbocatión después de un proceso de oxidación-reducción consecutivos fue un gran descubrimiento. Tras la demostración de la existencia de este intermedio mediante estudios de fotólisis de destello de láser, el siguiente paso fue extender esta metodología tanto como fuera posible. Las aminas alílicas están presentes en numerosos productos naturales y fármacos con actividad anti-fúngica, anti-bacterial y anti-inflamatoria. Además fue posible utilizar también como nucleófilos alcoholes y heterociclos ricos en electrones para formar los correspondientes productos Z– y E– alilados. Aunque la actividad biológica de los compuestos E- es bien conocida, creemos que el acceso a los correspondienbtes compuestos Z– abrirá nuevas vías para futuras investigaciones.
Fig. 2 Propuesta de mecanismo para la reacción de alilación (izquierda) y estudios de fotólisis de destello láser (derecha).
Contacto
José Alemán, Responsable de grupo FRUAM en FotoArt-CM – jose.aleman@uam.es
Coordina FotoArt-CM: Víctor A. De la Peña O´Shea. IMDEA Energía.
Más información