![]()
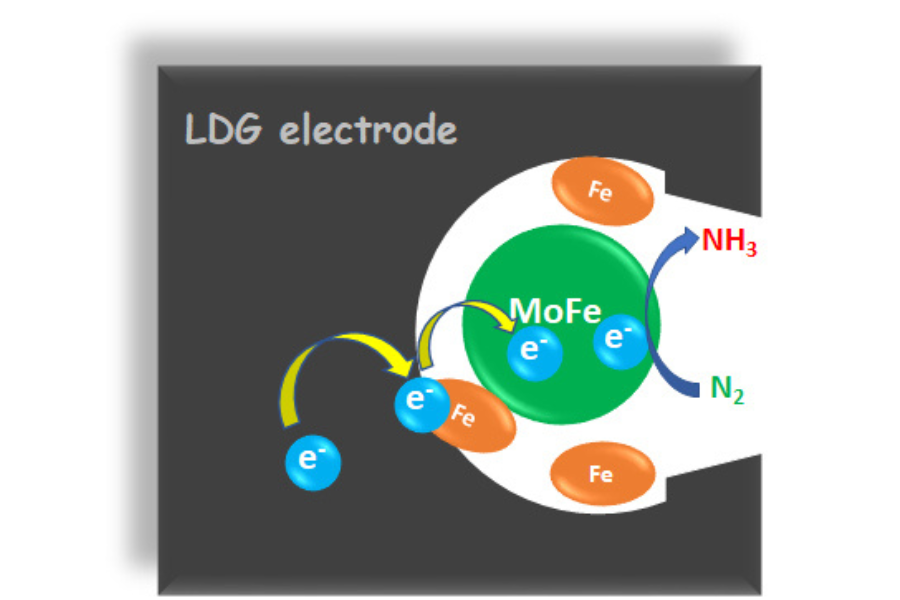
Enzimas que catalizan la producción de amoniaco a partir del nitrógeno atmosférico.
La enzima nitrogenasa cataliza la reducción de nitrógeno a amoniaco en condiciones suaves de reacción, pudiendo utilizar directamente electricidad para este proceso de síntesis.
Antonio López de Lacey. Instituto de Catálisis y Petroleoquímica. CSIC
Una de las reacciones más importantes de la industria química es la reducción de nitrógeno atmosférico a amoniaco. El amoniaco es un compuesto químico esencial para la elaboración de productos de limpieza, como reactivo en la producción de fármacos y sobre todo para la fabricación de fertilizantes agrícolas. Aproximadamente 185 millones de toneladas de amoniaco se producen anualmente en el mundo, principalmente por el proceso de Haber-Bosch. Este proceso desarrollado en el siglo XIX fue fundamental para el desarrollo de la revolución industrial y también para la agrícola, ya que permitió la fabricación masiva de fertilizantes que incrementaron exponencialmente la producción de alimentos, favoreciendo por tanto el incremento de la población mundial. El proceso de Haber-Bosch implica la reacción de los gases nitrógeno e hidrógeno a muy altas temperaturas y presiones para obtener como producto amoniaco. Por este motivo se trata de uno de los procesos químicos que más energía demanda y principal causante de las emisiones de dióxido de carbono (CO2) de origen industrial, suponiendo alrededor del 3% de las emisiones totales de este gas de efecto invernadero. Por lo tanto, es fundamental desarrollar procesos químicos más sostenibles para la síntesis de amoniaco mediante la disminución del consumo energético empleado para la reacción [1].
Una vez más, la naturaleza puede ser fuente de inspiración para el desarrollo de alternativas más sostenibles para la producción de amoniaco. Hay microorganismos que son capaces de fijar el nitrógeno atmosférico para producir el amoniaco necesario para su metabolismo. Para este fin disponen de enzimas capaces de catalizar la reducción del triple enlace del nitrógeno molecular (N2) a amoniaco (NH3) [2]. Las nitrogenasas de MoFe son las más activas catalíticamente y estudiadas. Están formadas por dos metaloproteínas: la proteína MoFe, donde el N2 se une y se reduce a NH3, y la proteína Fe, que transfiere los electrones necesarios para la reacción catalítica formando complejos transitorios con la proteína MoFe. La barrera energética de activación para conseguir la reducción de nitrógeno a amoníaco se supera a expensas de la hidrólisis de 16 moléculas de trifosfato de adenosina (ATP), un cofactor biológico que proporciona energía para impulsar muchos procesos en las células vivas, por cada 2 moléculas de NH3 producidas [3]. Son numerosos los estudios científicos para estudiar la síntesis biológica de amoniaco utilizando electricidad para proporcionar los electrones necesarios para la reducción del nitrógeno a amoniaco, ya sea utilizando microorganismos fijadores de nitrógeno o directamente las nitrogenasas que contienen. En la mayoría de estos estudios se utilizan mediadores redox, es decir compuestos químicos que transportan los electrones desde el electrodo al enzima, para facilitar el proceso electro-enzimático. Recientemente, García-Molina y cols. del Instituto de Catálisis y Petroleoquímica (CSIC) y del Centro de Biotecnología y Genómica de Plantas (UPM/CSIC) han reportado un avance importante en la producción electro-enzimática de amoniaco al conseguir la transferencia directa de electrones a la enzima nitrogenasa mediante el atrapamiento conjunto de sus dos proteínas componentes en grafito poroso de baja densidad. Este material conductor tiene una estructura porosa formada por macroporos que permiten la rápida de difusión de los reactivos a través de él, y de mesoporos de un diámetro entre 10 y 50 nm adecuado para atrapar ambas proteínas de la nitrogenasa en el electrodo, facilitando la transferencia directa de electrones para la reacción enzimática de producción de amoniaco [4].
La producción de amoniaco por métodos (foto)electrocatalíticos es uno de los objetivos del proyecto FotoArt5.0-CM (TEC-2024/TEC-308) del Programa de Actividades de I+D en Tecnologías 2024 de la Comunidad de Madrid, en el cual participa el grupo FCA del Instituto de Catálisis y Petroleoquímica del CSIC. El uso de nitrogenasas, o de compuestos biomiméticos, como electrocatalizadores es de interés para conseguir este objetivo.
Bibliografía
- D. Milton, S. Cai, S. Abdellaoui, D. Leech, A. L. De Lacey, M. Pita, S. D. Minteer. Angew. Chem. Int. Ed. 56, 2680-2683, 2017.
- Lopez-Torrejon,, F. Jiménez-Vicente, J. M. Buesa, J. A. Hernández, H. K. Verma, L. M. Rubio. Nat. Commun. 7, 11426, 2016.
- Einsle. Current Op. Struct. Biol. 83, 102718, 2023.
- García-Molina, C. Echavarri-Erasun, M. del Barrio, S. González-García, L. M. Rubio, M. Pita, Al. De Lacey. Electrochim. Acta 529, 146342, 2025.