![]()
Oxidación de hidrógeno en medio alcalino: Ni/N-CNT
Autor: Manuel Montiel. Universidad Autónoma de Madrid
Las pilas de combustible son dispositivos capaces de transformar en energía eléctrica y de manera efectiva la energía química almacenada en combustibles como hidrógeno o alcoholes de baja masa molecular. Dentro de las pilas de combustible, las que operan a baja temperatura (~100 ºC), han sido tradicionalmente dispositivos de membrana polimérica que trabajan en medio ácido. Para llevar a cabo el proceso electroquímico se han empleado catalizadores de Pt o metales del grupo del platino (PGMs), tanto para la oxidación de combustibles en el ánodo como para la reducción de oxígeno en el cátodo. Pero el empleo de nuevos dispositivos de membrana polimérica que trabajan en medio básico ha permitido abrir el abanico de catalizadores que se pueden emplear, tanto en el ánodo como en el cátodo [1]. Sin embargo, mientras que para el cátodo se han conseguido catalizadores con actividad comparable a la del Pt, solo algunos PGMs (Pt, Ir, Pd…) presentan una actividad adecuada para la oxidación de hidrógeno en medio alcalino, donde la reacción es más lenta.
Una alternativa al empleo de PGMs como ánodos en pilas de hidrógeno alcalinas son los catalizadores basados en níquel, como aleaciones de NiMo, NiTi o NiCoMo, o también nanopartículas de níquel decoradas con óxidos metálicos. Aunque la actividad de estos materiales es inferior a la obtenida con PGMs, se pone de manifiesto la posibilidad de abaratar los costes de las pilas de combustible de hidrógeno en medio alcalino. Recientemente Zhongbin Zhuang y colaboradores han presentado un trabajo en el que se describe la síntesis y caracterización de nanopartículas de Ni soportadas sobre nanotubos de carbono dopados con N (Ni/N-CNT) y con las que logran una actividad comparable a la del Pt en las mismas condiciones de medida [2]. Aunque los nanotubos de C dopados con N (N-CNT) tienen una actividad frente a la oxidación de hidrógeno tan baja como los nanotubos de carbono sin dopar (CNT), su empleo como soporte produce un efecto sinérgico que no se observa con estos últimos.
En este trabajo se llevaron a cabo cálculos DFT (Density Functional Theory) con dos modelos de nanopartículas cuboctaédricas de Ni (Ni13 y Ni37), investigando el efecto de la localización de los átomos de N en relación con la nanopartícula (en el centro: Nc, o en los bordes: Ne). Se observó que los clúster de Ni sin soportar o soportados sobre CNT presentan una distribución de energías de enlace Ni‑H más amplia, lo que implica mayor heterogeneidad de sitios a los que se une el H, además de que la unión a dichos sitios es más fuerte en la mayoría de los casos. Mientras, en los modelos con carbono dopado no se observan energías tan altas. Estas diferencias tienen un origen tanto electrónico (debido a transferencias de carga) como geométrico (relajación del clúster).
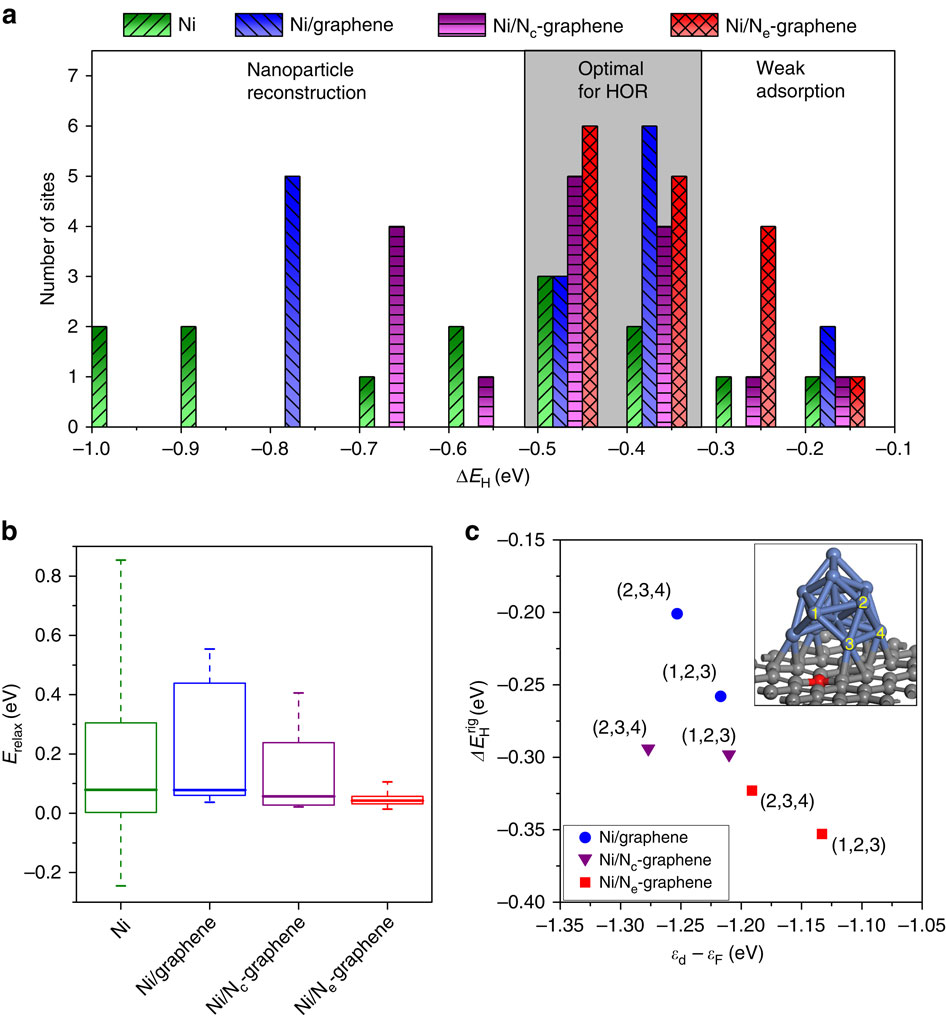
(a) Distribution of site-dependent hydrogen-binding energies for each model system. (b) Distribution of relaxation energies for each model system on hydrogen-binding to each site. (c) Shifts in the d-band centre with respect to the Fermi level and binding energy at adjacent Ni sites (1,2,3) and (2,3,4).
Zhuang, Z. et al. Nickel supported on nitrogen-doped carbon nanotubes as hydrogen oxidation reaction catalyst in alkaline electrolyte. Nat. Commun. 7:10141 doi: 10.1038/ncomms10141 (2016)
Los cálculos teóricos también indican que los átomos de N que interaccionan con el centro de la nanopartícula (Nc) producen una relajación de la estructura del clúster de menor grado que para Ni o Ni/CNT, mientras que los Ne producen una relajación con una reconstrucción mínima de la estructura, relacionado con la menor fortaleza de los enlaces Ni-H que se forman. Estos efectos electrónicos y estructurales se traducen en una mayor activación de los centros implicados frente a la reacción de oxidación de hidrógeno. Así mismo, estos cálculos predicen que tamaños más pequeños de nanopartículas podrían proporcionar mayor actividad frente a esta reacción, debido a un mayor número de interacciones Ni-Ne. Como se muestra en la siguiente figura, los cálculos teóricos predicen de buen grado los resultados obtenidos para la densidad de corriente de intercambio en la reacción de oxidación de hidrógeno.
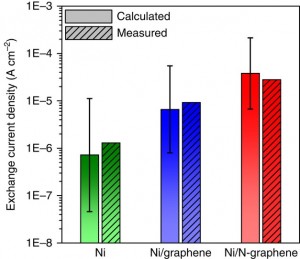
Unpatterned bars are the calculated exchange current densities and patterned bars are the measured values. The calculated exchange current density of Ni/Ne-graphene is shown for Ni/N-graphene. Error bars are 75% confidence intervals resulting from the regression of the volcano relationship in Supplementary Equation 2.
Bibliografía
[1] Montiel M. Materiales carbonosos dopados con N como catalizadores para pilas de combustible. 2016.
[2] Zhuang Z, Giles SA, Zheng J, Jenness GR, Caratzoulas S, Vlachos DG, et al. Nickel supported on nitrogen-doped carbon nanotubes as hydrogen oxidation reaction catalyst in alkaline electrolyte. Nature Communications. 2016;7:10141. This work is licensed under a Creative Commons Attribution 4.0 International License: http://creativecommons.org/licenses/by/4.0/