![]()
MÁS DE CRISPR
La tecnología conocida como CRISPR, a la que ya nos referimos en un blog anterior, constituye uno de los mayores logros de la comunidad científica que ha revolucionado las perspectivas de la edición y regulación genómica por su capacidad de generar (modificar y manipular) cambios en el genoma de una célula de forma coordinada y precisa, teniendo por ello potenciales usos en campos muy diversos.

Entre las innumerables aplicaciones que posee esta herramienta podemos citar las siguientes:
– Desarrollo de modelos celulares y animales para el estudio de enfermedades, así como para la preparación y ensayo de nuevas terapias.
– Cribado genómico con el objetivo de averiguar la función de regiones del genoma.
– Control epigenético, relativo a las variaciones hereditarias mitóticas y/o meióticas en la expresión génica que no son causadas por cambios en la secuencia del ADN.
– Obtención de imágenes en vivo del genoma celular.
– Tratamiento y diagnóstico de enfermedades, tanto genéticas como no genéticas.
– Usos en los sectores agrícola y ganadero para, por ejemplo, obtener nuevas variedades de plantas o animales más seguros y productivos.
Todas estas utilizaciones de la edición basada en CRISPR han sido objeto de numerosas patentes durante estos últimos años, algunas de las cuales comentamos a continuación:
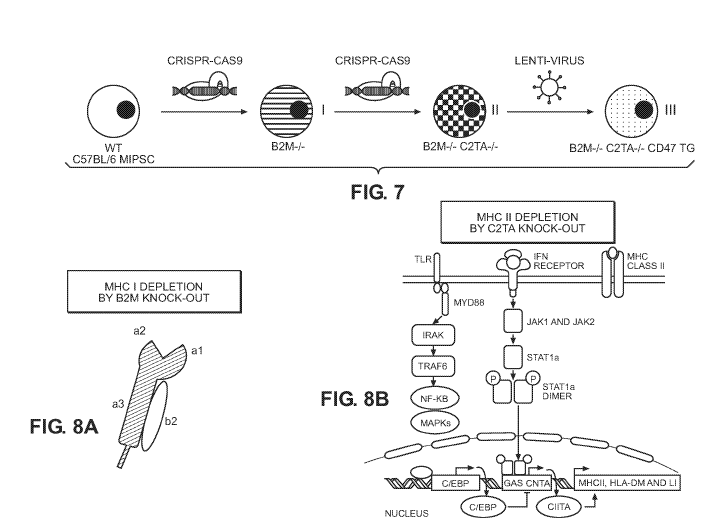
WO2018132783 expone la obtención de células madre pluripotentes hipoinmunogénicas, es decir, células modificadas de tal forma que evitan el rechazo inmunológico del huésped cuando son utilizadas en terapia celular regenerativa. Esto se logra reduciendo la expresión de la beta-2-microglobulina (B2M) y del transactivador del complejo mayor de histocompatibilidad clase II (CIITA) e incrementando la expresión del clúster de diferenciación CD47. Se trata de células que carecen de importantes antígenos inmunitarios y que están diseñadas para evitar la fagocitosis.
WO2018195402 describe el uso de la tecnología CRISPR para obtener cerdos libres de retrovirus endógenos. Estos animales modificados genéticamente podrían ser utilizados en xenotrasplantes de forma más fiable, teniendo en cuenta que los órganos porcinos son más adecuados, en comparación con los de otros animales, por ser similares a los órganos humanos tanto en tamaño como en función. Se evita con ello, no sólo la transmisión de retrovirus endógenos porcinos a las células humanas sino, además, otras enfermedades que pueden causar la integración de estos retrovirus, como la inmunodeficiencia y el cáncer.
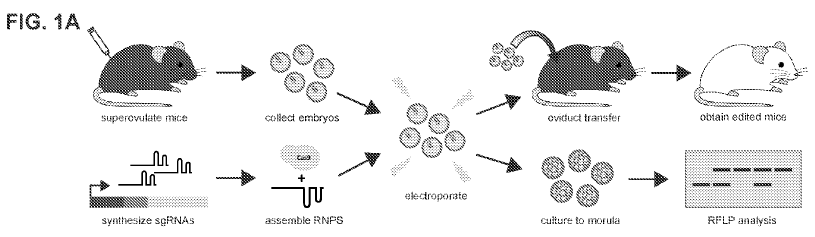
WO2017173092 se dirige a métodos para modificar el genoma de un cigoto de mamífero utilizando el sistema CRISPR. La molécula de ADN genómico diana puede ser alterada mediante sustitución y/o inserción y/o eliminación de uno o más nucleótidos. En muchos casos, se trata de genes involucrados en diversas enfermedades, por ejemplo porque presenten mutaciones que hacen que el péptido que codifican no sea funcional o sea sintetizado en una cantidad inferior a la normal.
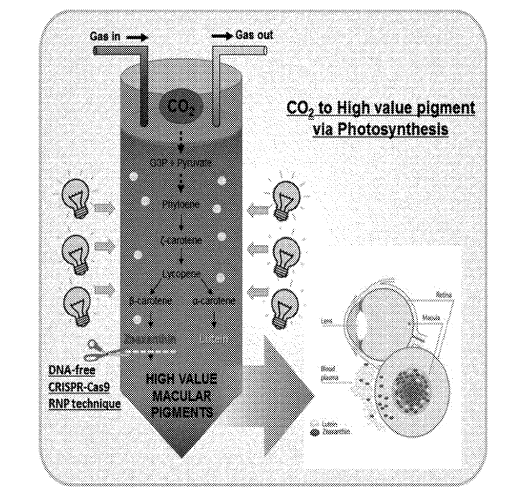
US2019045812 tiene por objeto unas microalgas mutantes de la especie Chlamydomonas reinhardtii, con mutaciones en el gen ZEP pero sin introducción de ADN exógeno, que poseen mayor capacidad de producir unos pigmentos derivados de los carotenoides denominados xantofilas, entre las que se encuentran la luteína y la zeaxantina, compuestos útiles para prevenir la degeneración macular, mantener la salud de la retina y mejorar la función ocular. Las microalgas obtenidas pueden ser cultivadas y utilizadas como materia prima en medicina o en alimentación.
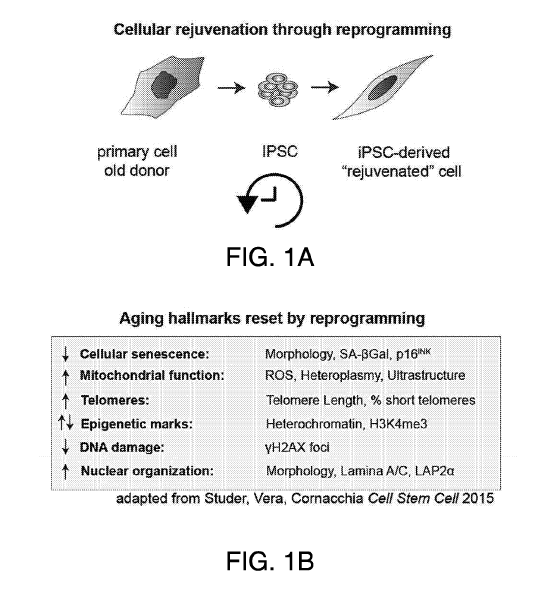
WO2018148667 se refiere a aquellos factores del envejecimiento fisiológico que se deben a cambios reversibles en el transcriptoma y el epigenoma de modo que, si se identifican, podemos modular una célula, por ejemplo, una célula en un cultivo, tejido o sujeto, para lograr un perfil transcripcional y epigenético característico de la edad cronológica temprana y, por lo tanto, «rejuvenecer» la célula, o bien para lograr un perfil transcripcional y epigenético de una edad cronológica tardía y, por lo tanto, «envejecer» la célula. Este método para reprogramar la edad celular comprende administrar a la célula un sistema de ingeniería epigenética consistente en un sistema CRISPR/Cas9 el cual altera una característica epigenética en una secuencia del genoma diana de la célula o bien la expresión de una secuencia del genoma diana de la célula.
WO2018001302 explica que el estrés abiótico, como son la disponibilidad de agua insuficiente o las temperaturas extremas, es la principal causa de pérdida de cultivos en todo el mundo. Para poder adaptarse a las diferentes condiciones ambientales, las plantas utilizan estrategias que implican cambios en la regulación de genes, en la morfogénesis y en el metabolismo, aunque esto también se puede lograr mediante la obtención de plantas modificadas genéticamente utilizando la herramienta CRISPR/Cas9, tal y como divulga esta patente. Así, modificando la expresión de ciertos genes se logran plantas con mayor tolerancia a la sequía, floración más temprana o mayor rendimiento de grano.

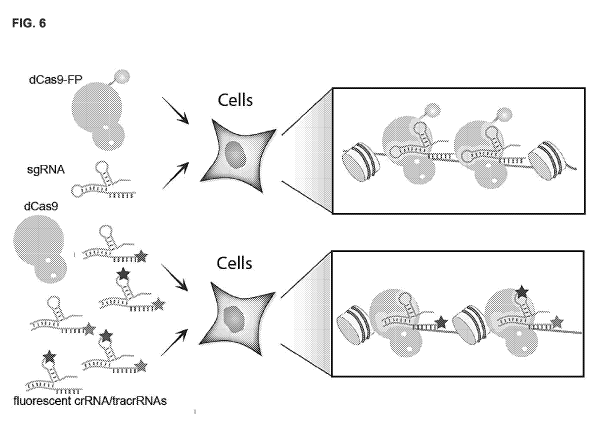
WO2018226575 detalla un método basado en la introducción de una ribonucleoproteína marcada mediante el sistema CRISPR/Cas para visualizar, detectar o aislar un ácido nucleico, de manera que se puede llevar a cabo un diagnóstico preciso en células vivas. Es un sistema con el que se pueden marcar loci endógenos, permitiendo así disponer de un diagnóstico rápido de anomalías genéticas y cromosómicas o visualizar la dinámica genómica, con aplicaciones también en el tratamiento de pacientes y en investigación.
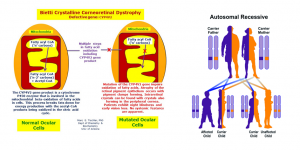
WO2019025984 anticipa modelos celulares y terapias para una enfermedad ocular autosómica recesiva sin tratamiento terapéutico efectivo, la distrofia cristalina de Bietti, que cursa con una progresiva pérdida de visión. Se han identificado numerosas mutaciones en el gen CYP4V2 que se asocian con la enfermedad y, así, el modelo celular consiste en una célula (célula madre o célula madre pluripotente inducida) en la que se introducen una o más mutaciones en el gen CYP4V2 mediante edición genética, pudiendo emplearse, así mismo, para evaluar la eficacia de un determinado agente terapéutico. Además, la edición genética mediante CRISPR podría utilizarse como terapia para la corrección, alteración o reemplazo del gen CYP4V2 o una porción del mismo.
Sin embargo, la tecnología CRISPR, que parte del descubrimiento de las secuencias CRISPR de bacterias realizado por el español Francisco Martínez Mojica, presenta riesgos que impiden su traslado a la práctica clínica, de modo que en la actualidad no puede ser utilizada directamente en pacientes. Además, la posibilidad de que pueda emplearse para fines considerados no apropiados, como es la creación de bebés modificados genéticamente, ha suscitado preocupaciones sociales y éticas.
Por otro lado, el 26 de junio de 2018 el Tribunal Europeo de Justicia consideró a los organismos obtenidos por mutagénesis como organismos modificados genéticamente (OMG). Esta sentencia, muy criticada por la comunidad científica, equipara los riesgos de estos organismos con los de los transgénicos, obligándoles a demostrar su seguridad y su toxicidad.
En cualquier caso, es indiscutible que se trata de una metodología muy versátil y sencilla con gran potencial, siendo previsible que en un futuro próximo se convierta en una herramienta mucho más segura y eficaz.