![]()
La Química en los medios de comunicación: el airbag
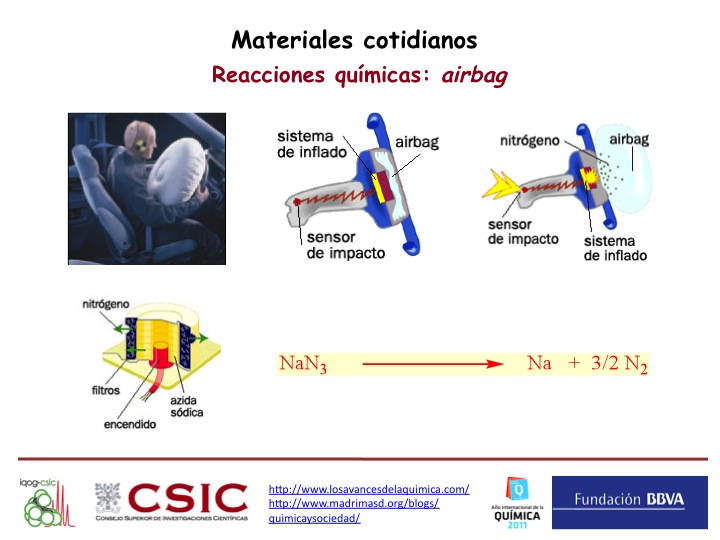
En la página web de RTVE «EL PORQUÉ DE LAS COSAS«, América Valenzuela explica el funcionamiento del airbag, que se basa en la descomposición de la azida sódica, un compuesto termodinámicamente estable, pero inestable cinéticamente (es decir, reactivo en ciertas condiciones) cuando se calienta, golpea o presiona, generando nitrógeno. La reacción es exotérmica (desprende calor) y en ella se genera un gas (nitrógeno) a partir de un sólido (azida sódica), aumentando considerablemente el volumen.
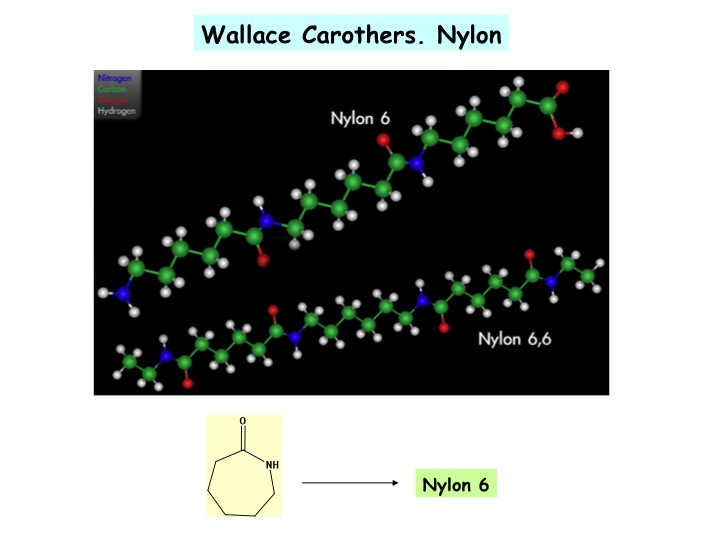
Las reacciones en las que se generan calor y se aumenta el volumen son la base de los explosivos. En el caso del airbag, la cantidad de azida sódica es muy pequeña y el airbag está protegido por un material químico (un polímero), el Nylon, muy resistente a la tensión; por eso, la «explosión» de azida sódica no rompe la bolsa en la que está contenida. El Nylon es uno de las sustancias químicas imprescindibles en nuestras vidas, con miles de aplicaciones. El Nylon fue sintetizado por primera vez por Wallace Carothers, uno de los más grandes genios de la Química del siglo XX.
Todos estos temas están siendo tratados en la II edición del curso de divulgación «Los avances de la Química y su impacto en la sociedad«. A continuación hay algunas imágenes de las charlas del curso en los que tratamos los temas del airbag y el Nylon.
Bernardo Herradón
IQOG-CSIC



no se por que nunca ponen una respuestas a nuestras necesidades como estudiantes le pedimos una cosa y salen con otra
¿Y cual es su necesidad?
Hola. Soy una estudiante de segundo de bachillerato, y tu publicación me ha servido de gran ayuda. Debo realizar un trabajo sobre el Airbag, pero no consigo encontrar información a una de las preguntas que debo responder. Dice así: «Las reacciones que se producen en el airbag provocan una ligera disminución de la temperatura, ¿qué quiere decir eso? ¿Beneficia este hecho al hinchado del cojín? ¿Por qué?»
Si lograra pudiera estaría muy agradecida.
¡Gracias!
La ligera disminución de la temperatura es debido a que la reacción es endotérmica; es decir que la entalpía de reacción es mayor que cero, lo que significa que absorbe energía del medio.
En la descomposición de la azida sódica se genera sodio metálico. Puesto que este es muy reactivo, dentro del airbag se añade un oxidante, generalmente nitrato sódico, que convierte el sodio en óxido de sodio. También se suele añadir sílice para que el óxido de sodio se convierta en silicato sódico, que es inocuo. La entalpía de la reacción global depende de la diferencia de entalpía de los compuestos iniciales iniciales (azida sódico y los aditivos, por ejemplo nitrato sódico y sílice) y de los productos finales de la reacción (nitrógeno, silicato, óxidos, etc.). Supongo que los fabricantes de airbag diseñarán los dispositivos para que no se caliente y, preferiblemente, para que se enfríe ligeramente.
Un Saludo cordial.
Les agradezco profundamente si me pueden ayudar con algo que estoy desarrollando, soy inventor pero no muy pilo en química.
¿Cómo puedo hacer para que el azida sódica reaccione a nitrógeno, pero al golpearla o presionarla o al mezclarla con otro compuesto químico pero sin generar gases tóxicos?.
Hola, amigo Herradón sus trabajos los utilice para mi trabajo de grado no solo en los antecendentes sino también en el marco teórico, excelente. Soy farmaceútica egresada de la Universidad Central de Venezuela, y docente integral, hice magister educacion mención química. Mi trabajo esta enfocado a la enseñanza de la química utilizando los aportes del periodismo cientifico. Ahora nos disponemos a elaborar un periódico dedicado a temas relacionados con la química. Gracias por sus aportes.
Muchas gracias por comentar.
Me alegro de que la información de este blog se a de utilidad.
Te animo a seguir también la web http://www.losavancesdelaquimica.com/
y el blog
https://educacionquimica.wordpress.com/
Así como los distintos sitios (paginas y grupos) de Facebook que gestiono.
Saludos.
Buenas, soy un estudiante de Educación Media General, y me han mandando una actividad, pero no la he podido conseguir en ningún sitio, si me podrían ayudar… por favor. Es «¿Cuales son los elementos o compuestos químicos en los medios de comunicación?»
Por favor, alguien que me ayude. Millón de agradecimientos.