![]()
Nuevo coronavirus SARS-CoV-2: Los test diagnósticos y para qué sirve cada uno
Hace unos días escribí un hilo en Twitter comentando lo básico acerca de los métodos diagnósticos de COVID-19. El hilo ha tenido una gran repercusión, por lo que creo que puede ser útil reproducirlo en este blog.
Parece que hay cierta confusión con las técnicas de diagnóstico y vigilancia de #COVID19. Voy a intentar explicarlo un poco. Abro hilo
Conviene empezar explicando algunas cosas: por lo general hay dos tipos de tests, o pruebas de laboratorio:
- Las que detectan el patógeno, en este caso el virus, o elementos propios de éste, como su genoma.
- Las que detectan anticuerpos que reaccionan frente al virus.
Las primeras pueden ser virológicas (aislamiento en cultivo), antigénicas (detección de antígenos del virus) o moleculares (detección del genoma del virus). Las segundas se conocen como «pruebas serológicas» porque se basan en la detección de anticuerpos en suero.
Entre las primeras, las más empleadas son las moleculares, por lo que en adelante nos centremos en éstas. Las famosas «PCR» (reacción en cadena de la polimerasa) pertenecen a esta categoría. Hay muchas otras, pero las PCR presentan tantas ventajas que dominan en el diagnóstico.
Las segundas (serológicas) son muy variadas en forma, pero para lo que nos interesa aqui podemos distinguir dos: el ELISA y la IC (inmunocromatografía), ésta última es uno de los «tests rápidos» de los que tanto se habla.
Por cierto, «Test rápido» es una denominación poco afortunada: hay muchos tests «rápidos», que emplean muchos formatos, y que sirven para detectar anticuerpos (son «serológicos») o virus (concretamente antígeno vírico). Por ahora no nos metemos en este tema.
De momento quedémonos con esto:
- La PCR (y tests análogos) detectan genoma del virus, y por lo tanto INFECCIÓN ACTIVA.
- Las pruebas serológicas detectan ANTICUERPOS, y por lo tanto reacción inmune frente al virus. Detecta que el virus ha infectado al individuo muestreado.
Además, hay otra cosa importante que hay que saber: una PCR positiva no implica necesariamente que el indivíduo contagie. Para eso se necesita un virus INFECCIOSO. Una PCR positiva puede provenir de restos del virus, o de virus neutralizados por anticuerpos, que no infectan.
Y si no infectan, no contagian. En conclusión NO TODAS LAS PCR POSITIVAS CORRESPONDEN A UNA FASE CONTAGIOSA DE LA INFECCIÓN.
Esto puede verse en el esquema que he preparado al efecto para el COVID19, basado en datos de estudios reales (ver referencias al final):
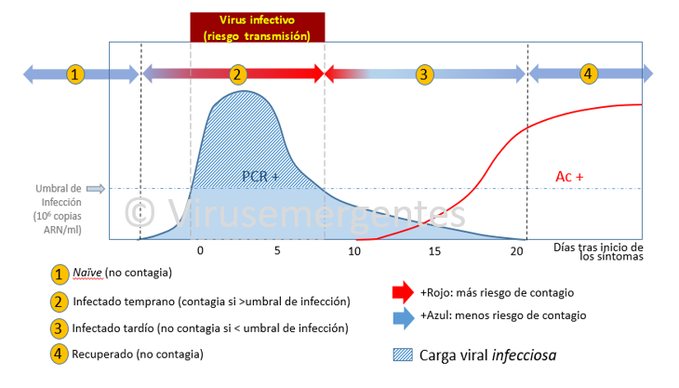
En este esquema puede verse que empleando PCR y una técnica serológica podemos clasificar a los indivíduos en 4 categorías con diferentes niveles de riesgo de contagio: 1) naïve; 2) Infectados tempranos; 3) infectados tardíos y 4) recuperados. (ACLARACIÓN: este esquema representa a los casos leves o asintomáticos, los casos clínicamente más graves tienen otras consideraciones que no vamos a abordar en este hilo).
Los casos asintomáticos y leves tienen gran importancia epidemiológica, pues son los que más contribuyen a la transmisión del virus. La atención sanitaria se ha centrado mucho en los casos graves, pero el control de la pandemia pasa por controlar los asintomáticos y leves.
Por ello ahora cobra una importancia inusitada el empleo de los dos tipos de técnicas, serológicas y moleculares. Hay aún lagunas y cuestiones técnicas que resolver, pero está claro que tenemos que emplear ambas estrategias para controlar esta enfermedad.
Se me olvidó decir que el contagio se produce en una ventana concreta de la infección. varios estudios señalan que es desde 2 dias antes a aproximadamente una semana después del incio de los síntomas (en los casos leves).
Por último, algunas referencias de la bibliografía empleadas en este hilo:
Mizumoto, K. et al, (2020). Estimating the asymptomatic proportion of coronavirus disease 2019 (COVID-19) cases on board the Diamond Princess cruise ship, Yokohama, Japan, 2020. Euro Surveill. 2020;25(10):pii=2000180.
Bai, Y., et al. Presumed Asymptomatic Carrier Transmission of COVID-19. JAMA (2020). https://doi.org/10.2807/1560-7917.ES.2020.25.10.2000180.
Aguilar, J. et al. Investigating the Impact of Asymptomatic Carriers on COVID-19 Transmission medRxiv 2020.03.18.20037994; doi: https://doi.org/10.1101/2020.03.18.20037994
He, X. et al. Temporal dynamics in viral shedding and transmissibility of COVID-19. medRxiv 2020.03.15.20036707; doi: https://doi.org/10.1101/2020.03.15.20036707.
Wölfel, R., Corman, V.M., Guggemos, W. et al. Virological assessment of hospitalized patients with COVID-2019. Nature (2020). https://doi.org/10.1038/s41586-020-2196-x
Zhao, J. Jr et al. Antibody responses to SARS-CoV-2 in patients of novel coronavirus disease 2019. medRxiv 2020 doi: https://doi.org/10.1101/2020.03.02.200301895
Zhang, W. et al. Molecular and serological investigation of 2019-nCoV infected patients: implication of multiple shedding routes, Emerging Microbes & Infections (2020) 9:1, 386-389, DOI: 10.1080/22221751.2020.1729071.
Wu LP, et al. Duration of antibody responses after severe acute respiratory syndrome. Emerg Infect Dis. 2007;13(10):1562–1564. doi:10.3201/eid1310.070576.
Bao, L. et al Reinfection could not occur in SARS-CoV-2 infected rhesus macaques. BioRxiv March, 2020. doi: https://doi.org/10.1101/2020.03.13.99022.Okba, N.M.A. et al. SARS-CoV-2 specific antibody responses in COVID-19 patients. MedRxiv, March 2020. doi: https://doi.org/10.1101/2020.03.18.20038059.
Corman, V et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveill. 2020;25(3):pii=2000045. https://doi.org/10.2807/1560-7917.ES.2020.25.3.2000045
