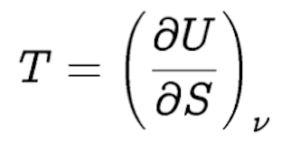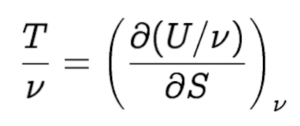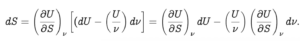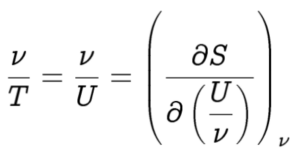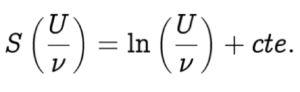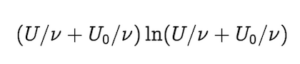![]()
El espectro de radiación de Planck no necesita hipótesis cuánticas
Lo que se necesita para determinar la dependencia de la energía de la radiación en función de frecuencia y temperatura son ligaduras, condiciones que limiten las posibilidades de esa dependencia. El primer principio es una de esas ligaduras: impone la conservación de la energía en la forma cambio de energía del sistema igual al calor recibido por el mismo menos el trabajo realizado a su vez por ese sistema. Pero esto nos deja aún con muchas posibilidades. El segundo principio, una segunda ligadura, exige que la variación de entropía del sistema (realmente, una combinación de magnitudes físicas, combinación sin realidad física), sin inyección de trabajo, sea siempre igual o mayor que cero, alcanzando un máximo cuando el sistema deja de evolucionar, cuando alcanza el equilibrio.
Estas dos leyes producen la regla de desplazamiento de Wien, la ligadura de que la entropía debe ser una función genérica de una única variable: el cociente entre la energía y la frecuencia, pero no permiten dar la forma explícita de la dependencia de la energía (o de la densidad de energía) en función de la frecuencia y la temperatura del emisor.
Para conseguir esto se precisa la tercera ligadura, la tercera ley, que nos dice que la entropía de cualquier sistema en el cero absoluto de temperatura, es cero. Planck no formuló esta tercera ley, pero podía haberlo hecho, pues ¿que otro valor podría tener la entropía en el cero absoluto de temperaturas?
La radiación EM dentro de una cavidad con paredes ennegrecidas tiene las mismas características que cualquiera de los átomos de esas paredes que absorben y emiten la tal radiación. Podemos considerar que uno de esos átomos es sencillamente un dipolo que radia mediante una oscilación de frecuencia ν. Puesto que el oscilador está dentro de un campo EM de una enorme gama de frecuencias (incluso una radiación supuestamente monocromática tiene una dispersión notable en frecuencia) el oscilador varía en Δν la suya. Si ese oscilador tiene una energía media U, el trabajo, cuyo icono es δW, que realiza al variar su frecuencia al oscilar es δW =(dU/ν) dν.
Recordemos que el calor (la energía deslocalizada en frecuencia de la radiación que mueve al oscilador) es δQ = dU – δW. Puesto que la entropía es por definición S=δQ/T, donde T es la temperatura del sistema a la que se intercambia el calor, la segunda lay de la termodinámica afirma que
dS = (1/T) (dU -δW) = (1/T)[dU -(U/ν)dν]
Ahora el problema es determinar T. La temperatura es un concepto estadístico, exige o bien multitud de objetos (átomos, partículas, compartiendo energía por interacción), o bien, en este caso, cambios constantes en la energía por cambios en la frecuencia del oscilador. Así podemos hablar de energía media en el tiempo <U> del oscilador y definimos, para T estrictamente mayor que cero y para sistemas que interactuando unos con otros, ya que acabo de afirmar que T es la temperatura a la que se intercambia calor, y así:
T = (1/kB)<U>
donde kB, adelantando conocimientos, es la constante de Boltzmann.
Ahora, la entropía solo puede ser una función de U y de ν (no hay más variables), y
o
y así
Invirtiendo la derivada parcial de U con respecto a S tenemos
e integrando
Tenemos aquí la forma funcional de la entropía de cualquier sistema, que es un logaritmo natural de algún argumento. Ahora tenemos que refinar esta expresión, pues según la misma, la entropía tiende a -∞ cuando U tiende a cero para una frecuencia distinta de cero, y sabemos que la entropía debe ser cero en el cero absoluto. La expresión de arriba es, evidentemente, válida solamente para energías U razonablemente altas.
Cuando la energía U decrece debe existir un valor de U/ν, distinto de cero, para el cual la entropía se haga nula, porque la entropía no puede tender a menos infinito, lo que ocurriría si la energía tendiese a cero, y con T igualmente haciéndose cero. Aparece aquí la energía de la temperatura cero o energía del punto cero. En el cero absoluto de temperatura, cada oscilador mantiene una energía que se puede poner como la constante de Planck U_0 = hν. Esta constante es así la menor energía posible de cada oscilador de un conjunto de ellos, cuando ninguno se mueve con respecto a los demás. Es una energía totalmente clásica que aparece sin demandar efectos cuánticos.
Por lo tanto la expresión para la entropía debe incluir un factor (U/ν – U_0/ν) que se hace 0 en el cero absoluto de temperatura, que multiplique al logaritmo, pero si solo ponemos esto, la entropía crecería como la energía al crecer ésta, y no como el logaritmo de la energía. Si restamos otro término tenemos
y ahora, introduciendo este término y desarrollando las ecuaciones llegamos al resultado
y obtenemos una expresión con los límites correctos.
Despejando para U
Aquí aparece el término (1/2)hν, que queda en la expresión de la energía cuando T se hace cero. Si ν es distinto de cero, los osciladores están vibrando, pero el desplazamiento neto es cero, y la temperatura solo se puede referir a la media de la energía cinética cuando hay desplazamiento neto.
El concepto de temperatura implica la interacción entre entes físicos. La diferencia de temperaturas provoca un flujo de energía en forma de calor. De aquí deducimos la idea de que la temperatura es la energía cinética media de un conjunto de entes (partículas, átomos, moléculas) interactuantes. En el cero absoluto, T=0K de temperaturas, no hay movimiento de interacción entre los entes, pero sí cada uno de ellos vibra por su cuenta. De ahí la energía del punto cero (1/2)hν.
La de arriba es la expresión deducida por Planck, echando mano de la teoría de combinaciones de elementos discretos, pero sin el término (1/2) h/ν, la energía de vibración de un oscilador inmóvil en el cero absoluto, la energía del punto cero, que como hemos visto, no es un efecto cuántico.
De nuevo, y como he especificado en los dos últimos posts, la mecánica atómica no necesita hipótesis cuánticas. La discretitud de todos los fenómenos a nivel atómico y macroscópico deriva de la estructura de la materia, como veremos en otro post.
Referencia: T.H. Boyer. Arxiv 1809.09093v1