La Asamblea General de Naciones Unidas, en su sesión A66/L.51, hecha pública el 15/06/2012 (www.un.org), decidió proclamar 2014 Año Internacional de la Cristalografía (IYCr2014, iycr2014.org). Entre varios considerandos, la resolución reconoce que la comprensión material de nuestro mundo se debe en particular a esta ciencia y subraya que la enseñanza y aplicación de la misma es fundamental para hacer frente a múltiples desafíos, esenciales para el desarrollo de la humanidad
| La Cristalografía ha hecho posible averiguar cómo son los cristales, las moléculas, las hormonas, los ácidos nucleicos, los enzimas, las proteínas y los virus, 'viendo' su estructura atómica en tres dimensiones |
La resolución, que hace justicia a 100 años de desarrollo imparable de la Cristalografía, congratula a todos los cristalógrafos, y en especial a todos aquellos especialistas que trabajan en España, quienes también colaboran con la Unión Internacional de Cristalografía en la preparación de actos conmemorativos y difusión de esta ciencia, gracias a la cual hemos podido fisgar en el mundo de los átomos y de las moléculas, y comprender su funcionalidad.

Belleza de los cristales
Cristales, ¿qué cristales?
La palabra 'cristal' contiene un cierto grado de perversión conceptual en nuestro idioma común, pues solemos asignar el nombre genérico de 'cristal? a los materiales que deberían designarse exclusivamente con el nombre de 'vidrio', situación que no ocurre en otros idiomas como el inglés, francés o alemán. Los vidrios de las ventanas los conocemos con el nombre cristales, y en las cristalerías sólo venden vidrios. La palabra 'cristal' debería, pues, referirse exclusivamente a materia ordenada, mientras que la palabra 'vidrio' designa materiales desordenados.
Cristales para magia, remedio y belleza
Las primeras referencias históricas sobre el uso de cristales provienen del cuarto milenio a.C., de los antiguos sumerios, pues parece probado que los usaban en fórmulas mágicas, quizá inducidos por sus peculiares formas externas. Y también tuvieron (y aún tienen) cierto uso se en la medicina tradicional china, hecho que parece remontarse al menos a 5.000 años atrás. Los antiguos egipcios hicieron también un uso muy extendido de minerales cristalizados; el lapislázuli, la turquesa, el rubí, la esmeralda y el cuarzo transparente como joyas, algunas piedras con fines protectores y garantía de salud, y algunos cristales (reducidos a polvo) con fines cosméticos, como la galena y la malaquita para sombra de ojos.

Cristales de proteína
¿Y qué es la Cristalografía?
¿Por qué el agua hierve a 100ºC y el metano a -161ºC?, ¿por qué la sangre es roja y la hierba es verde?, ¿por qué el diamante es duro y la cera es blanda?, ¿por qué los glaciares fluyen y el hierro se endurece al golpearlo?, ¿cómo se contraen los músculos?, ¿cómo la luz del sol hace que las plantas crezcan y cómo los organismos vivos han sido capaces de evolucionar hacia formas cada vez más complejas? ... Las respuestas a todos estos problemas han venido del análisis estructural. Con estas palabras, y refiriéndose a la Cristalografía, se expresaba Max F. Perutz (Laureado Nobel de Química, 1962) en julio de 1996, según consta en los archivos del Churchill College, Cambridge (UK).
La Cristalografía es la ciencia que explora el micro-mundo de los átomos a una resolución increíblemente detallada. Ha hecho posible que podamos averiguar cómo son los cristales, las moléculas, las hormonas, los ácidos nucleicos, los enzimas, las proteínas y los virus, 'viendo' su estructura atómica en tres dimensiones. Pero, más aún, con sus resultados podemos comprender a qué se deben las propiedades de todos estos materiales y/o compuestos, y podemos entender su funcionalidad en una reacción química, en un tubo de ensayo, o en el interior de un ser vivo.
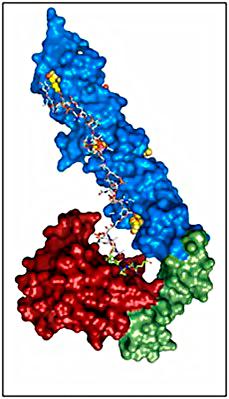
Estructura de una proteína
Gracias al conocimiento que nos proporciona la Cristalografía somos capaces de producir materiales con propiedades prediseñadas, desde catalizadores para una reacción química de interés industrial, hasta pasta de dientes, placas de vitrocerámica, materiales de gran dureza para uso quirúrgico, o determinados componentes de los aviones, por poner algunos ejemplos. Gracias a la Cristalografía conocimos los secretos estructurales del ADN, el llamado código genético. Podemos aumentar la resistencia de las plantas frente al deterioro medioambiental. Somos capaces de comprender, modificar o inhibir, enzimas implicados en procesos fundamentales de la vida e importantes para mecanismos de señalización que ocurren en el interior de nuestras células, como el cáncer. Gracias al conocimiento de la estructura del ribosoma, la mayor fábrica de proteínas de nuestras células, podemos entender el funcionamiento de los antibióticos y modificar su estructura para mejorar su eficacia. Estamos aprendiendo de la estructura de ciertos componentes de los virus para combatir bacterias con alta resistencia a antibióticos, y somos capaces de desentrañar las maquinarias de defensa tan sutiles que han desarrollado estos gérmenes, con lo que podremos combatirlos con herramientas alternativas a los antibióticos.
Con estas capacidades, la Cristalografía se ha convertido en una disciplina básica de muchas ramas científicas, desde la Mineralogía y la Geología hasta la Ciencia de Materiales, Química, Nanotecnología, Bioquímica, Biología y Biomedicina. Pero además, la Cristalografía ha favorecido y se ha enriquecido a través de la interacción con otras disciplinas, tales como la Física, la Ingeniería y las Matemáticas, siendo por tanto una de las ciencias más multi- e interdisciplinares existentes, enlazando diferentes áreas de investigación frontera.
Sugerimos al lector interesado en estos temas visitar la información contenida en la web que se ofrece desde el Departamento de Cristalografía y Biología Estructural (CBE) del Instituto de Química-Física 'Rocasolano' (CSIC).

Morfología de un copo de nieve
¡Y todo comenzó con un copo de nieve!
Si la Cristalografía ha sido capaz de llevarnos a este grado de conocimiento sobre la estructura de la materia, y por ende a su comprensión, los cimientos sobre los que descansa la Cristalografía moderna hay que encontrarlos en los matemáticos del siglo XVII y en concreto al trabajo de Johannes Kepler (1571-1630), quien fue consciente de que los copos de nieve que aterrizaban sobre su chaqueta siempre mostraban una perfecta simetría de seis puntas, y que éstos nunca aparecían con cinco, o siete puntas. A Kepler le siguieron otros estudiosos, como el danés Niels Stensen (1638-1686) y el francés Jean-Baptiste Louis Romé de l'Isle (1736-1790) quien formuló matemáticamente las observaciones de Stensen sobre la constancia de ángulos entre las caras de los cristales.
La teoría sobre la estructura cristalina que elaboró Haüy en 1784, basada en sus planteamientos sobre las leyes de la Simetría, de los Índices Racionales y de la Constancia de Ángulos entre Caras, no difiere sustancialmente, de los conceptos que prevalecen hoy en día sobre el conocimiento morfológico de los cristales. De dicha teoría se deriva el concepto de repetición de pequeñas unidades ('celdillas elementales') que, como ladrillos, se apilan en las tres direcciones del espacio dando lugar al sólido cristalino, siendo el ordenamiento repetitivo el responsable de las peculiaridades morfológicas que ostentan estos cuerpos.
El desarrollo de las Matemáticas de principios del siglo XIX propició que el médico alemán Johann Friedrich Christian Hessel (1796-1872) demostrara que, como consecuencia de la Ley de los Índices Racionales formulada por Haüy, las diferentes morfologías cristalinas se combinaban para dar exactamente 32 tipos de simetría en el espacio euclidiano, es decir, 32 'grupos puntuales' (32 combinaciones de elementos de simetría que pasan por un punto del centro del sólido cristalino), y que éstas son las únicas combinaciones compatibles con la repetición de ladrillos elementales introducida por Haüy.
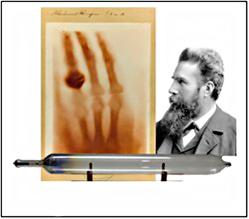
W.C. Röntgen (1845-1923)
En 1848 el físico francés Auguste Bravais (1811-1863) demostró matemáticamente que sólo podían existir 14 redes únicas en los sistemas cristalinos tridimensionales. Y finalmente, las 14 redes de Bravais y los 32 grupos puntuales de Hesse fueron las limitaciones entre las que se movieron el cristalógrafo ruso Evgraf S. Fedorov (1853-1919) y, de forma independiente, el matemático alemán Arthur Schönflies (1853-1928), para deducir entre 1890 y 1891 los 230 posibles grupos espaciales que restringen la distribución repetitiva de las unidades de construcción de los cristales (átomos, iones y moléculas), poniendo el punto final a toda la teoría vigente sobre la geometría y simetría de los retículos sobre los que se fundamentan los cristales.
¿Y cuáles fueron los orígenes de la Cristalografía moderna?
La resolución de la ONU coincide con el centenario de uno de los hallazgos más llamativos de la ciencia, la constatación de que los rayos X, descubiertos en 1895 por Wilhelm Conrad Röntgen (1845-1923), se comportaban como ondas electromagnéticas y, lo que fue aún más importante, que éstos interaccionaban con los cristales, a través del fenómeno denominado difracción, demostrando la constitución repetitiva de estos últimos. Tales descubrimientos (1912), que fueron debidos al físico alemán, y laureado Nobel de Física en 1914, Max von Laue (1879-1960), fueron seguidos por un conjunto de nuevos hallazgos que cambiaron nuestro conocimiento sobre la materia, y por ende la historia contemporánea.
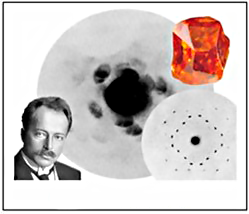
Max von Laue (1879-1960)
Muchos de los científicos que han sido responsables del desarrollo de la Cristalografía moderna obtuvieron el Premio Nobel, pero, injustamente, no todos lo fueron. Sin embargo, aun así, la Cristalografía ha producido, directa o indirectamente, el mayor número de laureados Nobel, 28, de la historia de estos premios. Muchos de estos grandes personajes han dejado una huella imborrable en la historia de esta ciencia. Unos ya se fueron, y otros siguen entre nosotros, pero con seguridad otros vendrán para mantener viva la 'melodía inacabada' con la que 'suena' esta ciencia que cada día se plantea retos más altos.
Como ejemplo de las posibilidades que ofrece esta ciencia sugerimos al lector que consulte la animación que se ofrece a través de este enlace y que muestra algunos hallazgos sobre la capacidad de camuflaje y virulencia de una temible bacteria conocida por todos, el Streptococcus pneumoniae.

