![]()
La alarma del verano de 2010: resistencia NDM-1
autor: Jesús Mingorance
Hospital Universitario La Paz. IdiPAZ.
A mediados de agosto aparecía en The Lancet un trabajo presentando la caracterización epidemiológica y molecular de una nueva resistencia a antibióticos llamada NDM-1, asociada a infecciones por bacterias gramnegativas. Con un tono algo menos neutro de lo habitual en la literatura científica, los autores advertían de los riesgos que puede entrañar su hallazgo, y esa advertencia ha levantado la alarma transmitida por diversos medios de comunicación, en los que se ha presentado como la nueva superbacteria que traerá el fin de la era de los antibióticos, etc. etc. Tanto es así que la revista Newsweek, que suele publicar una sección titulada «sabiduría popular» (Conventional Wisdom), en su número doble de agosto atribuía a la resistencia NDM-1 el mismo índice de preocupación que al virus VIH, mientras que rebajaba los índices de otros virus causantes de gripes, tanto la A como la aviar, y de neumonías como el SARS que han alarmado a la opinión pública en el último lustro.
Y lógicamente, nos preguntamos ¿de qué va todo esto? ¿qué tiene de particular la dichosa resistencia de la bacteria? ¿…? Intentaremos dar algunas respuestas.
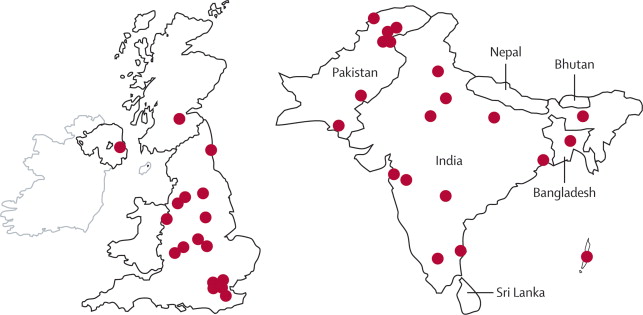
Distribución de las estirpes de enterobacterias conteniendo la resistencia NDM-1 en Bangladesh, India, Pakistan, y el Reino Unido. (fuente: REFERENCIA).
¿Qué quiere decir NDM-1 y por qué es peligroso? En primer lugar conviene aclarar que, contrariamente a lo que indican algunos titulares, NDM-1 no es una bacteria. Es una proteína y más concretamente una metalo-β-lactamasa (metalo-beta-lactamasa ó MBL). Esto quiere decir que NDM-1 es una enzima, una proteína que tiene actividad catalítica. Las MBLs reciben este nombre porque tienen uno ó dos átomos de zinc en su centro activo, y actúan rompiendo el anillo beta-lactámico de los antibióticos de la familia de la penicilina (con la única excepción del aztreonam). La rotura del anillo desactiva completamente el antibiótico. Además, como las demás MBLs, NDM-1 es insensible a los inhibidores de beta-lactamasas de uso clínico corriente, como el ácido clavulánico. Muchas veces el ácido clavulánico se asocia a los tratamientos con los antibióticos del tipo de la penicilina precisamente para evitar que las betalactamasas presentes en muchos patógenos los inactiven sin más. Esto quiere decir que una infección producida por una bacteria productora de NDM-1 no podrá tratarse adecuadamente con ningún antibiótico beta-lactámico (penicilinas, cefalosporinas, carbapenems), ni con ninguna de las combinaciones de antibiótico más inhibidor que se utilizan habitualmente.

Estructura de una metalo-beta-lactamasa de la bacteria Pseudomonas aeruginosa. Las dos esferas amarillas son dos átomos de zinc en el centro activo. (fuente).
¿Y cual es el problema? ¿acaso no hay otros antibióticos? Sí, hay otras familias de antibióticos a las que no les afecta NDM-1. El problema es que esta resistencia anula por si sola a casi toda la familia de los beta-lactámicos, que constituyen una parte muy importante del arsenal antibacteriano, y que por sus propiedades son los antibióticos preferidos para tratar la mayor parte de las infecciones. El problema es también que la resistencia está asociada a un elemento genético transferible, es decir, que puede viajar entre diferentes clones de una especie, e incluso entre diversas especies, y por lo tanto puede llegar a una bacteria que ya tenía previamente otras resistencias. Esto ocurre con facilidad en los hospitales, donde la presión antibiótica es muy elevada, y el resultado es la selección de clones multirresistentes, que con frecuencia son muy difíciles de tratar. De hecho, varias de las cepas descritas en el trabajo de Kumarasamy y colaboradores son multirresistentes, y una de ellas es pan-resistente (“resistente a todo”).
¿Qué me pasaría si fuese portador de una bacteria productora de NDM-1? Nada. Lo más probable es que no se diera cuenta. Nuestra flora bacteriana está formada por muchas bacterias, entre las que se encuentran las enterobacterias. La NDM-1 es una proteína que puede encontrarse en enterobacterias y les confiere resistencia a los antibióticos, pero no tiene ninguna actividad tóxica ni virulenta. La colonización por bacterias productoras de NDM-1 no es peligrosa en sí misma. El problema surge cuando alguna de estas bacterias produce una infección por lo difícil que puede resultar tratarla.
¿Y entonces, qué me pasaría si tuviese una infección por una bacteria productora de NDM-1? En la mayoría de los casos podría utilizarse un tratamiento antibiótico alternativo. Si la bacteria responsable es multirresistente las opciones de tratamiento pueden estar seriamente limitadas, y aquí entran en juego otros factores, como el tipo de infección, el microorganismo y el estado basal del paciente. No es lo mismo una infección urinaria que una neumonía, ni es lo mismo una infección en un paciente que previamente estaba sano, que en un paciente que ya tenía algún otro problema. En general con los tratamientos alternativos hay menos experiencia de uso y, en ocasiones pueden ser más tóxicos, lo que puede dificultar el tratamiento, especialmente en pacientes “frágiles”.
¿Si tuviese una infección por una bacteria productora de NDM-1 me la detectarían? Los análisis rutinarios de los Servicios de Microbiología incluyen antibiogramas. Si un paciente tiene una infección por una bacteria productora de MBLs se detectará dicha actividad y se dará esa información a su médico. Para determinar si se trata de NDM-1 o de otra MBL habrá que analizar el gen que codifica la resistencia (mediante PCR, por ejemplo). Dado que todas las MBLs tienen actividades similares la identificación precisa del gen es de interés epidemiológico, pero no es relevante para el paciente.
¿Y no pueden utilizarse antibióticos nuevos? Sí, hay algunos antibióticos aprobados recientemente que parecen funcionar bien, pero ninguno es de una familia nueva. El problema es que la investigación en esta área se ha reducido mucho en las últimas décadas, las líneas en desarrollo son muy escasas y es previsible que en los próximos años salgan al mercado muy pocos nuevos antibióticos. El pozo se está secando, desde hace ya algún tiempo se vienen lanzado mensajes al respecto, pero la reacción está siendo lenta y tímida (en el mejor de los casos).
¿Pero hay motivos para alarmarse? No y sí. No hay motivos para generar una alarma inmediata. La aparición de NDM-1 no supone realmente una novedad, las MBLs se describieron ya en la década de los noventa, y aún son poco frecuentes. Sin embargo, desde su descubrimiento se han expandido por todo el mundo y su frecuencia va en aumento, y eso sí es preocupante porque nos estamos quedando sin armas para responder.
¿De dónde viene NDM-1? Se trata de un gen natural que por su actividad particular ha sido seleccionado por la presión antibiótica sobre la flora bacteriana humana. Al integrarse en un elemento genético móvil capaz de saltar entre cepas, e incluso entre especies, se difunde muy rápidamente. No conocemos las funciones originales de las MBLs, pero deben estar relacionadas con el metabolismo de la pared bacteriana. El análisis de las secuencias de aminoácidos de las diferentes familias de MBLs indica que están lejanamente emparentadas, lo que a su vez muestra que se trata de un grupo de enzimas antiguo y ampliamente distribuido entre las enterobacterias. (Lo siento, no hay fundamentos para teorías conspirativas).
Entonces, ¿dónde está la novedad? El título del trabajo de Kumarasamy y colaboradores sugiere que se ha descubierto un nuevo mecanismo de resistencia, y en ese sentido es incorrecto. Lo que se ha descubierto es un nuevo gen perteneciente a una familia ya conocida y cuyos mecanismos de acción han sido bien caracterizados. La novedad podría estar en la velocidad con la que NDM-1 está diseminándose por el mundo. En 2008 se detectan los primeros casos en Reino Unido, y en 2009 ya constituyen el grupo mayoritario, siendo el 40% de las MBLs detectadas (que son pocas en términos absolutos, pero están en aumento). Dado que se trata de la primera vez que se describe, aún no existen datos sobre otros países, aunque es previsible que en los próximos meses aparezcan ya los primeros informes.
¿Por qué ha surgido NDM-1 en la zona de la India y Pakistán? No hay ninguna razón objetiva. Otras familias de MBLs han sido descritas originalmente en Japón, Italia, Alemania, Brasil y Corea, y algunas de ellas se han diseminado ya por todo el mundo. El problema de las resistencias es un problema global. Sin embargo, sí es cierto que en los países en los que los antibióticos pueden comprarse sin receta médica (como la India, entre otros muchos…) suele hacerse un uso excesivo e innecesario de antibióticos que no benefician a nadie, pero que contribuyen a aumentar la presión antibiótica y a seleccionar resistencias. Por ello es más frecuente que las resistencias se originen en éstos países, y por ello volvemos a insistir en lo importante que es evitar el USO INNECESARIO de todos los antibióticos
REFERENCIA:
Kumarasamy KK, Toleman MA, Walsh TR, Bagaria J, Butt F, Balakrishnan R, Chaudhary U, Doumith M, Giske CG, Irfan S, Krishnan P, Kumar AV, Maharjan S, Mushtaq S, Noorie T, Paterson DL, Pearson A, Perry C, Pike R, Rao B, Ray U, Sarma JB, Sharma M, Sheridan E, Thirunarayan MA, Turton J, Upadhyay S, Warner M, Welfare W, Livermore DM, Woodford N.2010. Emergence of a new antibiotic resistance mechanism in India, Pakistan, and the UK: a molecular, biological, and epidemiological study. Lancet Infect Dis. 10: 597-602.

Excelente artículo de un tema (uno más) que dio pie a demasiados titulares sensacionalistas. Enhorabuena a Jesús por explicarlo tan bien.
(Me rechinan los dientes cada vez que leo la palabra «superbugs» en un titular de prensa, grrr…)
Muy claro,sacandole sensacionalismo al tema ( buen docente ,eh ).
El problema de la resistencia es grave, pero lo es tambien el de los laboratorios que no investigan mas porque no le es rentable a corto plazo.
Saludos
Es posible que esta superbacteria, sea capaz de mezclar su material genetico con otras bacterias y así crear un imperio del mal de superbacterias y que puedan eliminar al ser humano.
Respuesta a Pablo Rafael Gumez.
Hola,
te recomiendo que leas el libro «Ni contigo ni sin tÍ. Guía para entender los microbios» reseñado en otro artículo de este foro:
http://www.madrimasd.org/blogs/microbiologia/2010/11/04/131062
y en EL PAÍS:
http://www.elpais.com/articulo/sociedad/Microbios/todos/elpepusoccie/20101112elpepusoc_11/Tes
Un saludo
Miguel
[…] Eliminar la infección en los enfermos sigue siendo difícil, se ha publicado que la bacteria parece ser sensible a antibióticos del tipo carbapenem, que son de los llamados betalactámicos. Si bien el genoma secuenciado contiene información para codificar betalactamasa, una enzima que, en cantidad suficiente puede inactivar algunos betalactámicos como la penicilina, los antibióticos de tipo carbapenem son mas refractarios a ella. Sin embargo existen otras bacterias que son resistentes a carbapenem debido a una betalactamasa especial, la metalo-beta-lactamase 1 (NDM-1). […]
[…] Eliminar la infección en los enfermos sigue siendo difícil, se ha publicado que la bacteria parece ser sensible a antibióticos del tipo carbapenem, que son de los llamados betalactámicos. Si bien el genoma secuenciado contiene información para codificar betalactamasa, una enzima que, en cantidad suficiente puede inactivar algunos betalactámicos como la penicilina, los antibióticos de tipo carbapenem son mas refractarios a ella. Sin embargo existen otras bacterias que son resistentes a carbapenem debido a una betalactamasa especial, la metalo-beta-lactamase 1 (NDM-1). […]
[…] entonces una amenaza? Como ya hemos comentado en casos anteriores, para la mayoría de las personas no, porque nunca vamos a necesitar un tratamiento con colistina. […]
[…] en anteriores ocasiones la propagación mundial de algunas resistencias a antibióticos como NDM-1 o mcr-1. No son las únicas, en lo que llevamos de siglo han surgido y alcanzado distribución […]
[…] beta-lactámicos de generaciones anteriores (penicilinas y cefalosporinas). La variante original, NDM-1, se describió en 2010, y desde entonces se ha expandido por todo el mundo, evolucionando y generando hasta hoy decenas de […]