![]()
Los metales pesados en las aguas residuales
Con este artículo se pretende dar una visión del problema medioambiental que supone la presencia de metales pesados en las aguas residuales.
[ERNESTO SIMON. Grupo de Fisicoquímica de Procesos Industriales y Medioambientales, FQPIMA. Universidad Complutense de Madrid]
Como constituyentes importantes de muchas aguas podemos encontrar un número importante de metales pesados aunque su cuantificación sea a niveles de traza. Cualquier catión que tenga un peso atómico superior a 23 (que corresponde al peso atómico del sodio) se considera un metal pesado; así, las aguas residuales contienen gran número de metales pesados diferentes. Entre ellos se puede destacar níquel, manganeso, plomo, cromo, cadmio, zinc, cobre, hierro y mercurio, entre otros. Todos ellos se encuentran catalogados en la Directiva Europea 96/61/CE IPPC (Ley 16/2002) como sustancias contaminantes que deben tenerse obligatoriamente en consideración para fijar valores límites de emisiones, aunque algunos de ellos son imprescindibles para el normal desarrollo de la vida biológica, y la ausencia de cantidades suficientes de ellos podría limitar, por ejemplo, el crecimiento de las algas.
Las fuentes habituales de aguas residuales que contienen grandes cantidades de metales como el cromo, cadmio, cobre, mercurio, plomo y zinc proceden, principalmente, de limpieza de metales, recubrimientos, curados, refino de fosfato y bauxita, generación de cloro, fabricación de baterías y teñidos. Los efectos que provocan sobre el medio ambiente son los siguientes: mortalidad de los peces, envenenamiento de ganado, mortalidad de plancton, acumulaciones en el sedimento de peces y moluscos.
Otra serie metales como el hierro, calcio, magnesio o manganeso también están presentes en aguas residuales de las industrias de metalúrgica, fabricación de cemento, cerámicas y bombeos de gasolina. Sus efectos, menos peligrosos que los anteriores, principalmente son el cambio en las características del agua: color, dureza, salinidad e incrustaciones.
Debido a su toxicidad, la presencia de cualquiera de ellos en cantidades excesivas interferirá en gran número de los usos del agua. El BOCM nº269 (1993) sobre vertidos líquidos industriales al Sistema Integral de Saneamiento establece los valores límites de los siguientes metales:
Cromo Total : 5 mg/L | Cromo Hexavalente: 3 mg/L |
Bario: 20 mg/L | Cadmio: 0,5 mg/L |
Cobre: 3mg/L | Hierro: 10 mg/L |
Manganeso: 2 mg/L | Mercurio: 0,1 mg/L |
Níquel: 10 mg/L | Plomo: 1 mg/L |
Zinc: 5 mg/L | |
En la siguiente tabla se recogen las EC50 de algunos de los anteriores metales obtenida mediante diferentes ensayos
de Ecotoxidad con microorganismos de referencia:
Metal | Organismo | EC50 (mg/L) | Referencia |
Cadmio | P.subcapitata V.fisheri | 65-74 17-452 7965 16500 | Guéguen y col.,2004 USEPA,2001 Guéguen y col.,2004 Blaise y col.,1994 |
Cromo IV | P.subcapitata V.fisheri | 40-900 13756 16000 | Guéguen y col.,2004 Guéguen y col.,2004 Blaise y col.,1994 |
Cobre | P.subcapitata V.fisheri | 12-19 12-917 580 150 500 | Guéguen y col.,2004 USEPA,2001 Guéguen y col.,2004 Blaise y col.,1994 Utgikar y col.,2004 |
Plomo | P.subcapitata V.fisheri | 1900-4600 122 160 | USEPA,2001 Guéguen y col.,2004 Blaise y col.,1994 |
Zinc | P.subcapitata V.fisheri | 55-79 45-2600 488 1200 1480 | Guéguen y col.,2004 USEPA,2001 Guéguen y col.,2004 Blaise y col.,1994 Utgikar y col.,2004 |
Debido a esta naturaleza tóxica, algunos metales pesados causan impacto negativo sobre los tratamientos biológicos convencionales, así como sobre los ecosistemas receptores. En la siguiente tabla se muestran los límites de concentración de algunos metales que inhiben el tratamiento biológico:
Sustancia | Concentración de inhibición (mg/L) |
Cadmio (Cd2+) | 2-5 |
Bicromato (CrO42-) | 3-10 |
Cobre (Cu2+) | 1-5 |
Niquel (Ni2+) | 2-10 |
Zinc (Zn2+) | 5-20 |
Es por ello que a menudo resulta conveniente medir y controlar las concentraciones de estas substancias. Las cantidades de muchos de estos metales pueden determinarse, a concentraciones muy bajas, empleando métodos instrumentales entre los que destacan la espectroscopía de emisión de plasma con detención óptica o con detención de masas y la espectroscopía de absorción atómica.
A continuación se comentan las técnicas generales para retirar metales pesados de las aguas residuales.
Precipitación química
Las operaciones de precipitación y sedimentación química, llevadas a cabo de manera independiente o en combinación con reacciones de oxidación-reducción, se utilizan ampliamente para la eliminación de metales.
Los agentes de precipitación habitual son: cal, sosa cáustica y sulfuros. En la siguiente tabla se recogen sus características:
| Cal, Ca(OH)2 | Sosa Cáustica, NaOH | Sulfuros, NaSH y FeS |
| Reactivo más barato | Más cara que la cal | Tratamiento eficaz a bajas concentraciones |
| Genera grandes volúmenes de lodos | Genera menos volúmenes de lodos básicos | Lodo aplicable a la recuperación de suelos |
| Los lodos normalmente son aplicables a la recuperación de suelos | Lodo aplicable a la recuperación de suelos | |
También se emplean carbonatos de sodio y de calcio para metales cuando su solubilidad correspondiente, dentro de un intervalo de pH, no es la suficiente para acudir a este tratamiento.
La siguiente figura muestra la solubilidad de varios hidróxidos y sulfuros metálicos en diferentes condiciones de pH.
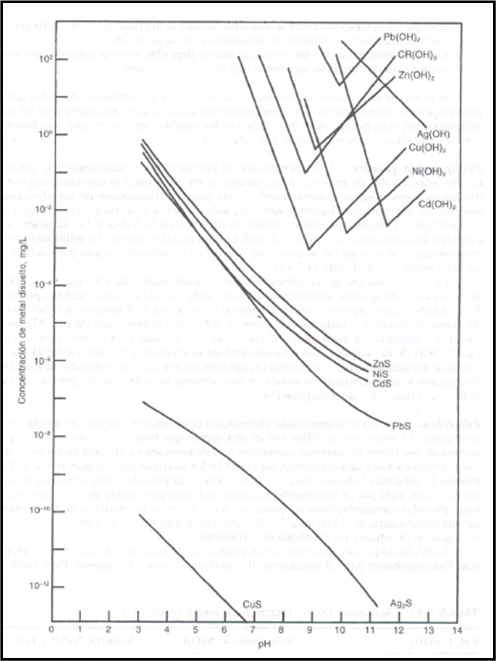
Una variante de la operación de precipitación es la precipitación electrostática, la cual se encuentra en vías de implantación a escala industrial.
La sedimentación puede ser sustituida por una filtración dependiendo del metal a tratar, así para el caso de retirar zinc, la precipitación química con cal se acompaña de una filtración en lechos de arena.
Para retirar cadmio, níquel o plomo suele adicionarse en la etapa de precipitación con cal un agente de captación para estos compuestos que está formado de silicatos, carbonatos y fosfatos de metales alcalinos. Esta adición además de obtener mayores rendimientos favorece la decantación.
Si se pretende retirar Zinc, Hierro, Cobre o Manganeso la cal empleada en la precipitación se puede sustituir por óxido de magnesio.
Intercambio Iónico
Para la eliminación de metales pesados en disoluciones diluidas resultan aplicables los sistemas de intercambio iónico. Las resinas que se emplean son resinas de intercambio catiónico, que se clasifican en fuertemente o débilmente ácidas.
Las resinas fuertemente ácidas presentan las siguientes selectividades (en orden decreciente de preferencia) hacia los diferentes cationes: bario, plomo, calcio, níquel, cadmio, cobre, zinc, magnesio, potasio, amoniaco, sodio e hidrógeno.
La ósmosis inversa constituye una alternativa para la eliminación de metales de corrientes residuales de bajo caudal.
Oxidación-Reducción
Las reacciones químicas de oxidación-reducción se emplean para reducir la toxicidad o la solubilidad, o para transformar una sustancia en otra más fácilmente manipulable. Como se ha visto con anterioridad esta operación mayoritariamente se combina con la precipitación química.
Las reacciones químicas de reducción se emplean principalmente para el tratamiento de corrientes que contiene cromo hexavalente, mercurio y plomo. Los agentes reductores más comunes son el dióxido de azufre, sales de sulfitos y sales de hierro.
Los procesos de reducción y precipitación de corrientes residuales que contienen cromo involucran una reducción del cromo hexavalente al estado trivalente en condiciones ácidas, pH £ 3, empleando dióxido de azufre como agente reductor, seguida de una precipitación con cal, en condiciones básicas, con pH entre 8 y 9:
H2Cr2O7 + 3SO2 ® Cr2(SO4)3 + H2O
Cr2(SO4)3 + 3Ca(OH)2 ®2Cr(OH)3+3CaSO4
Referencias
· Documento BREF de la IPPC: Mejores Técnicas Disponibles en Sistemas Comunes de Tratamiento/Gestión de Aguas y Gases Residuales en el Sector Químico (2003).
· Ingeniería de Aguas Residuales, Metcalf & Eddy, 3ra Edición Ed. McGraw-Hill, 1999.
· Manual de Referencia de la Ingeniería Ambiental, R.Corbitt, Ed. McGraw-Hill, 1999.
· Toxicity of metals and metals mixtures: analysis of concentration and time dependence for zinc and copper, V.P. Utgikar y col.,Water Research 38 (2004) 3651-58.
· Water toxicity and metal contamination assessment of a polluted river: the
· USEPA 2001. User guide: ECOTOXicology Database System.
· A bacteria toxicity assay performanced with microplates, microluminometry and Microtox reageant, Blaise y col., Biotechniques 16, 932-7.

Se<podra usar las membranas de osmosis inversa para reducir el volumen deaguas que contienen cromo hexavalente de 100-300 ppm y 600-800 ppm de SDT
pregunta: la osmosis inversa es capaz de reducir ARSENICO de 0.5 ppm a 0.1 ppm en un caudal de 0.1 l/s ?? …..quizás la pregunta debiera ser qué instalación de osmosis inversa ($$$) puede lograr esto?
felicitaciones por este esfuerzo!
Hola quisiera que me envien informacion acerca de la recuperacion de plata (Ag) a traves del proceso de osmosis inversa y si es posible darle algun uso a esta una vez se ha realizado el proceso
informacion acerca de como limpiar una laguna artificial contaminada con desechos industriales de plomo y zinc
gracias!
solicito informacion sobre tratamiento de aguas residyales con contenido de metales pesados
Me gustaría q me recomendaran libros o documentos en pdf sobre la contaminación de suelos por metales pesados.
Gracias
hola, quisiera saber si es posible utilizar la osmosis inversa para un caudal de 4500 galones/minuto.
Buenas:
Nose si mi duda esta fuera de sus competencias,aunq agradeceria la aclaración. Hoy ha estado una persona en casa mostrandome el veneficio de una depuradora con cautro filtros de carbono y una menbrana de osmosisi inversa. Tomo una muestra del agua del grifo y otra del agua embotellada q tomamos en casa. Introdujo un aparato parecido a una resistencia (q elevo la Tª) y las aguas tomaron unos colores amarillentos-anaranjados q despues precipitaron,incluso con olor a metal oxidado. Una vez intalada la depuradora de prueva y realizando la misma operación el aguq resultante apenas variaba el tono.Mi agua de red proviene de desaladora. Mi duda es la fiabilidad de lo q he visto. Si esas pruevas demuestran la calidad de mi agua. Espero respuesta. Gracias
Buenas:
Nose si mi duda esta fuera de sus competencias,aunq agradeceria la aclaración. Hoy ha estado una persona en casa mostrandome el veneficio de una depuradora con cautro filtros de carbono y una menbrana de osmosisi inversa. Tomo una muestra del agua del grifo y otra del agua embotellada q tomamos en casa. Introdujo un aparato parecido a una resistencia (q elevo la Tª) y las aguas tomaron unos colores amarillentos-anaranjados q despues precipitaron,incluso con olor a metal oxidado. Una vez intalada la depuradora de prueva y realizando la misma operación el aguq resultante apenas variaba el tono.Mi agua de red proviene de desaladora. Mi duda es la fiabilidad de lo q he visto. Si esas pruevas demuestran la calidad de mi agua. Espero respuesta. Gracias
hola me gustaria saber si se puede hacer un solo tratamiento las aguas servidas y aguas de mina espero respuesta adios
HOLA PARA HACER UN SOLO TRATAMIENTO DE AGUAS SERVIDAS Y AGUAS VERTIDAS DE LA MINA QUE METODO ES RECONDABLE GRACIAS
Hola quisiera saber para que se emplean los metales pesados, que es ycomo se realizan los procesos de datacion del tiempo con C14, resonancia magnetica nuclear, determinacion de la geometria nuclear
Hola:
quisiera saber para que se emplean los metales pesados,
que es ycomo se realizan los procesos de datacion del tiempo con C14,
resonancia magnetica nuclear,
determinacion de la geometria molecular
Hola, me gustaria saber si dispones de este articulo en formato PDF
hola quisiera consultar si saben de alguna experienca exitosa de biorremediación de metales pesados. desde ya les agradezco.
Hola quiero saber si conocen experiencias de tratamiento de aguas residuales que contienen metales pesados, utilizando algún tipo de algas marinas
quisiera saber la mejor alternativa para eliminar cobre, zinc, aluminio, hierro de agua corriente, que se utiliza para uso acuicola, en donde por lo general se reusa esta agua, por lo que requiere que el proceso de eliminación de estos metales pesados no debe dejar residuales que alteren la calidad normal del agua.-
Saludos
mauricio
holaaa, quisiera que me brinden información de archivos y/o documentos en Pdf sobre el «análisis del magnesio por el método de absorción atomica en el campo de metalurgia» graciasssssssssssssssss
ola de pura casualidad no sabes donde puedo descargar el libro de metcalf
hola que tal. trabajo en un sistema de bombeo de aguas servidas, (negras) fuera de la UE, pero me interesa adquirir información sobre los criterios se que utilizan en la UE para el manejo de este tipo de aguas, sobre todo con respecto a la protección del personal, equipos, sustancias a las que se exponen, riesgo biológico y químico, así como saber si existen trabajos de investigación que analicen todos estos riesgos con una exposición prolongada en el tiempo. Como aclaración diré que aquí llegan todas las aguas negras y pluviales de una ciudad de 2 millones de habitantes (salvo algunos efluentes industriales que son tratados en otras instalaciones). No se realizan tratamientos químicos a las aguas antes de ser bombeadas mar adentro, solamente se retiran elementos grandes por filtrado de rejas y parte de las grasas y arenas por decantado en un proceso de 5 minutos por gravedad.
hola, soy universitario desarrollo mi tesis con respecto al tema de los metales pesados en cuerpos de aguas naturales, pero se me ha dificultado conseguir informacion confiable sobre las correlaciones de los metales con factores como pH,profundidad del cuerpo de agua y con la temperatura del agua. muchos autores estudian a cada uno por separados pero muy pocos he conseguido que estudien la interaccion de estos metales con estos factores, espero puedan ayudarme!!
Excelente aporte. Muchas gracias por la informacion!.