![]()
Una alternativa para el tratamiento de las aguas residuales de la industria cosmética: el proceso de oxidación Fenton
Las aguas residuales de la industria cosmética se caracterizan por la presencia de una alta carga orgánica, que se traduce en una elevada demanda química de oxígeno (DQO), de la cual, una fracción importante corresponde a materia no biodegradable, que, por tanto, no responde bien a los tratamientos biológicos. El tratamiento de este tipo de efluentes tradicionalmente se ha llevado a cabo mediante procesos de flotación y coagulación-floculación, alcanzándose en general reducciones significativas de
[Grupo de Procesos y Sistemas de Ingeniería Ambiental, Universidad Autónoma de Madrid]
La creciente intensificación de la actividad humana en los tres grandes sectores económicos ha producido un efecto cada vez más importante sobre el medio ambiente. El aumento en la actividad industrial lleva inexorablemente asociado un incremento en el volumen de residuos, los cuales, si no son tratados adecuadamente, terminan contaminando el entorno, afectando a la calidad del aire, de las aguas y de la flora y fauna terrestre, pudiendo incluso llegar a afectar a la salud humana.
Entre los problemas medioambientales, la contaminación de las aguas adquiere una especial relevancia, debido a que se trata de un bien relativamente escaso, utilizado de forma intensiva, especialmente en los últimos años. Como consecuencia de la creciente preocupación social por el medio ambiente, la legislación referente a la calidad del agua está siendo cada vez más restrictiva.
A diferencia de las aguas urbanas, en las que la mayoría de los compuestos orgánicos son fácilmente biodegradables, el tratamiento de las aguas industriales puede complicarse por contener compuestos difíciles de degradar biológicamente (recalcitrantes o refractarios) o cuya degradación biológica se produce tan lentamente que hace ineficaz este tipo de tratamiento (compuestos persistentes), o incluso tóxicos para los microorganismos. Por lo tanto, son muchos los casos en los que se requieren tratamientos más específicos y avanzados.
Las aguas residuales procedentes de la fabricación de cosméticos, se caracterizan por la presencia de una alta carga orgánica, que se traduce en una elevada demanda química de oxígeno (DQO), así como por altos niveles de sólidos en suspensión, grasas y aceites, y detergentes. Esta situación merece una consideración especial, derivada del hecho de que una fracción importante de
El tratamiento de este tipo de efluentes tradicionalmente se ha llevado a cabo mediante procesos de flotación y coagulación-floculación con diversos agentes, como FeCl3 o Al2(SO4)3. En ocasiones estos tratamientos se han combinado con el empleo de carbón activo. En general, se han alcanzado reducciones significativas de
Los procesos de oxidación avanzada (POA’s) surgen como una alternativa para el tratamiento de este tipo de efluentes, debido a su potencial para degradar, parcial o totalmente, compuestos orgánicos refractarios. Entre los procesos de oxidación avanzada, uno de los más efectivos es el proceso Fenton, consistente en el empleo de H2O2 y sales de Fe2+ en medio ácido para promover la descomposición catalítica del H2O2 produciendo radicales HO·, los cuales son capaces de oxidar la materia orgánica y compuestos inorgánicos, como sulfuros, presentes en el agua residual. El esquema de reacción es el siguiente:
En presencia de sustancias susceptibles de reaccionar con los radicales HO·, otro posible esquema para la regeneración del catalizador (Fe2+) es:
El proceso es potencialmente útil para destruir contaminantes, ya que es muy efectivo para la generación de radicales HO·. Un exceso de iones Fe2+ puede atraparlos, al igual que los halógenos, el H2O2 o el radical perhidroxilo, afectando negativamente al proceso de oxidación:
Fe2+ + HO· –> Fe3+ + HO– k: 3,2.108 M-1·s-1
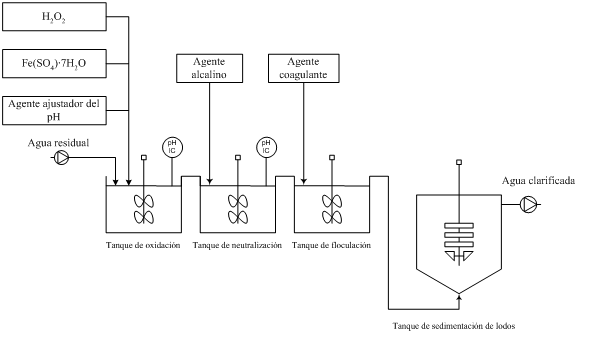
La aplicación del proceso Fenton para el tratamiento de aguas residuales presenta ventajas debido, por un lado, a la disponibilidad y bajo coste del Fe, elemento no tóxico, y por otro, a la facilidad de manejo del H2O2 y su descomposición en productos inocuos para el medio ambiente. Otra de las ventajas que presenta este proceso es que no se forman compuestos clorados como en otras técnicas de oxidación, y no existen limitaciones de transferencia de materia, por tratarse de un proceso homogéneo. La instalación necesaria es muy sencilla, generalmente un reactor tipo tanque agitado, y no es preciso emplear equipos adicionales para la generación de los reactivos, como ocurre en el caso del ozono o la radiación UV, lo que lo convierte en una de las alternativas más económicas. Asimismo, no es necesario suministrar energía extra para activar el H2O2, pudiendo trabajar a presión atmosférica y temperatura ambiente. Los puntos débiles más importantes del proceso Fenton son el elevado coste del H2O2 y el hecho de que, al tratarse de un proceso homogéneo, el hierro incorporado se pierde con el efluente, lo que, además, hace obligada la separación del mismo, que normalmente se lleva a cabo por precipitación como Fe(OH)3, en la etapa final de neutralización.
Si bien la reactividad inicial es función de la concentración de Fe2+, el rendimiento del proceso (o grado de mineralización) depende, entre otros factores (temperatura, pH, concentración de catalizador y de H2O2), de la reducción de Fe3+ a Fe2+, por lo que la regeneración del Fe2+ presenta una gran importancia. Además, no todos los compuestos orgánicos reaccionan con el radical HO· a la misma velocidad, sino que la reactividad del sistema Fenton es función de la naturaleza de los compuestos orgánicos presentes. En cualquier caso, está limitada por la presencia de Fe2+ y, por lo tanto, por el poder reductor de los intermedios de oxidación. Por otro lado, existen intermedios de reacción que en lugar de reducir el Fe3+ forman complejos con él, eliminándolo del ciclo Fe2+/Fe3+, reduciendo y/o inhibiendo la oxidación.
El sistema Fe2+/Fe3+/H2O2 presenta su máxima actividad catalítica a pH 2,8-3,0. Un incremento o disminución en este valor del pH reduce bruscamente la eficacia. Para valores de pH > 3-4, el Fe3+ precipita como Fe(OH)3 y descompone el H2O2 preferentemente a O2 y H2O. Además, la formación de complejos de Fe(II) a valores altos de pH conduce a la disminución de la concentración de Fe2+. Por otro lado, para valores de pH más ácidos, la regeneración del Fe2+ por reacción del Fe3+ con el H2O2 se ve inhibida.
Otro factor que tiene una gran importancia es la temperatura. Presenta dos efectos contrapuestos. Por un lado, un aumento favorece la cinética del proceso pero también disminuye la estabilidad del H2O2, cuya velocidad de descomposición a O2 y H2O aumenta alrededor de 2,2 veces por cada
La dosis de catalizador empleada y la concentración de H2O2 son dos factores que determinan la cinética del proceso. Ambas variables se encuentran relacionadas entre sí. Además, la concentración de H2O2 necesaria está igualmente ligada con la concentración inicial de contaminante. Se suelen emplear cantidades referidas a la relación estequiométrica, entendida como la cantidad teórica de H2O2 necesaria para oxidar el contaminante a CO2 y H2O.
La no selectividad del proceso lo convierte en un método capaz de eliminar compuestos orgánicos de diversa naturaleza. Son muy pocos los compuestos resistentes al ataque de este reactivo, entre los que cabe citar la acetona, el ácido acético, el ácido oxálico, las parafinas y algunos alcanos clorados (tetracloroetano, tricloroetano).
Este tratamiento se puede aplicar no sólo a aguas, sino también a lodos y suelos contaminados. Los principales efectos que se consiguen con el mismo son:
· Destrucción de los contaminantes orgánicos
· Reducción de la toxicidad
· Mejora de biodegradabilidad
· Reducción de
· Reducción del olor y color

La reaccion Fenton es muy efectiva para destruir moléculas complejas que no son biodegradables, no sólo de la industria cosmética, sino también en la industria farmacéutica, química e inclusive lixiviados de vertederos. FMC Foret en Barcelona ha desarrollado un proceso denominado OHP (Oxidación Húmeda con Peróxido) para el tratamiento de sustancias orgánicas no biodegradables o inclusive tóxicas. Está basado en Fenton también como indica el artículo. Pero en este caso, es a alta temperaturas (110ºC) y presiones (1,5 bar). Con esto logran acelerar la oxidación y reducir los tiempos de residencia (es un proceso continuo) a menos de una hora. Tienen varias plantas en operación en distintasa industrias.
Hola, primero dar las gracias a Francisco por ampliar la información, y para otros usuarios que les interese el tema, la página web del proceso OHP es http://www.fmcforet.com/Environment/OHP/tabid/2657/Default.aspx
Aquí encontraréis más información, y si no os funciona el link probar por la web de la empresa: http://www.fmcforet.com
Los felicito por su blog , muy , muy interesante vuestros artículos. Acabo de encontrar un artículo sobre un tema que debo investigar para mi Maestria de CCAA en La UNALM de Lima Peru.
asímismo se encuentra información valiosa de parte de los comentaristas.
Nuevamente FELICITACIONES.