![]()
PROCESO INTEGRADO DE COAGULACIÓN-FENTON PARA EL TRATAMIENTO DE AGUAS RESIDUALES INDUSTRIALES
Un novedoso proceso integrado de coagulación-Fenton se ha utilizado para el tratamiento de un efluente de agua residual de una industria de cosméticos situada en la Comunidad de Madrid. En un primer paso, FeSO4 se usó como coagulante y el Fe2+ no precipitado que permaneció en disolución se utilizó como catalizador para el posterior proceso Fenton. El proceso de coagulación alcanzó un notable decrecimiento del Carbono Orgánico Total (COT) sin que la concentración de compuestos fenólicos variase significativamente. Sin embargo, esta notable disminución de la carga orgánica produjo una considerable reducción de la cantidad de H2O2 requerida en el proceso Fenton para la eliminación de los fenoles. La integración de ambos procesos permitió el cumplimiento de los límites de vertido establecidos por la Ley 10/1993 de la Comunidad de Madrid para vertidos industriales a la red de saneamiento (a partir de Perdigón-Melón et al., 2010).
[Departamento de Química Analítica, Química Física e Ingeniería Química. UAH]
Las industrias de cosméticos como consecuencia de su actividad económica generan importantes volúmenes de efluentes residuales caracterizados por sus altos valores en Demanda Química de Oxígeno (DQO). El cumplimiento de la estricta legislación obliga a estas industrias al tratamiento de sus efluentes para conseguir una reducción tanto en su carga orgánica como en otros contaminantes inorgánicos antes de su descarga a cauce o a una red de saneamiento. A pesar de que los procesos de tratamiento biológico son más económicos que los físico-químicos, la alta carga orgánica de sus efluentes, ecotoxicidad o presencia en ellos de compuestos biorrecalcitrantes produce una baja relación DBO5/DQO que imposibilita su tratamiento a través de ellos (Bautista et al., 2007).
Entre los procesos físico-químicos, la coagulación ha recibido una considerable atención debido a su alta eficacia en la eliminación de DQO así como su elevada eficiencia en costes. Sin embargo, la eficacia de este proceso en la eliminación de DQO varía tanto con la naturaleza de los compuestos orgánicos como con las características físico-químicas del agua a tratar, especialmente alcalinidad o dureza (Tomaszewska et al., 2004). En particular, los fenoles son difícilmente eliminados en el proceso de coagulación y como resultado de ello, su concentración puede exceder los límites de vertido establecidos por la legislación. Para incrementar la eficacia de degradación de éstos, se ha propuesto integrar el proceso Fenton a continuación del de coagulación. Este método de oxidación se basa en el uso de la mezcla de Fe2+/H2O2 en condiciones ácidas para la generación de una elevada concentración de radicales hidroxilo, característica particular que define los procesos de oxidación avanzada (POA). El proceso Fenton ha sido ampliamente estudiado tanto en la degradación de derivados fenólicos como en el tratamiento de aguas residuales de industrias cosméticos (Lin et al., 1999; Bautista et al., 2007). Sin embargo, la elevada DQO típicamente encontrada en los efluentes de estas industrias requiere del uso de elevados volúmenes de un reactivo costoso como es el H2O2, hecho que podría limitar su aplicación práctica (Esplugas et al., 2002).
En este trabajo se llevo a cabo el estudio del proceso integrado coagulación-Fenton en el tratamiento de un efluente de una industria de cosméticos.
Material y métodos
El agua residual industrial se obtuvo del efluente de una empresa de preparación de productos cosméticos situada en la Comunidad de Madrid. Las principales características físico-químicas del agua residual así como los límites de vertido establecidos por la Ley 10/1993 de la Comunidad de Madrid para vertidos industriales a la red de saneamiento se muestran en la Tabla 1.
 a Valores máximos instantáneos para los Vertidos Líquidos Industriales al Sistema de Saneamiento de acuerdo a la Ley 10/1993 de la Comunidad de Madrid.
a Valores máximos instantáneos para los Vertidos Líquidos Industriales al Sistema de Saneamiento de acuerdo a la Ley 10/1993 de la Comunidad de Madrid.
El proceso experimental de coagulación se llevo a cabo en un dispositivo “Jar Test” (Selecta) utilizando volúmenes de 400 ml del efluente a tratar. Los coagulantes utilizados fueron: sulfato de hierro (FeSO4·7H2O, ≥99%, Sigma-Aldrich) y hidróxido de calcio (Ca(OH)2, ≥90%, Panreac). Los coagulantes se mezclaron con el agua residual vigorosamente (200 rpm) durante 5 minutos, seguida de una mezcla lenta (30 rpm) durante 30 minutos y un período sin agitación de 10 minutos.
El proceso Fenton se llevo a cabo con alícuotas de 50 ml de agua sobrenadante procedente del de coagulación. El efluente a tratar se acidificó hasta un pH de 2,7±0,2 con HCl (1M) y se adicionó H2O2 (33%, p/v, Panreac). La concentración inicial de peróxido de hidrogeno se fijó de acuerdo a la cantidad estequiométrica teórica (2,12 g H2O2/g DQO) establecida por Bautista et al. (2007). Las muestras se agitaron en un agitador orbital durante 240 minutos a temperatura ambiente y posteriormente el pH se ajusto a 8,0±0,5.
Se analizó la DQO, COT, DBO5, concentración de fenoles y hierro así como la inhibición de la luminiscencia de la bacteria Vibrio fischeri del agua residual bruta y tratada.
Resultados
Como se observa en la Tabla 1, el efluente de la industria a estudio incumple los límites de vertido de varios parámetros físico-químicos establecidos por la Ley 10/1993 de la Comunidad de Madrid: pH, DQO, Fenoles totales y Ecotoxicidad.
Proceso de Coagulación
El proceso de coagulación usando FeSO4 se evaluó en busca de las condiciones óptimas de pH y dosis de coagulante. Las menores valores de carga orgánica se alcanzaron a pH>8, sin diferencias significativas en el rango 8-10. El valor final de COT en el efluente clarificado fue de 200 mg l-1 (DQO=680 mg l-1). A pH=8, dosis de 2,29 g l-1 de FeSO4 optimizan el uso del coagulante al alcanzar la mayor reducción de materia orgánica por gramo de sal de hierro. Como contrapunto, en ninguna de las condiciones estudiadas de pH y dosis de FeSO4se encontraron reducciones significativas en la concentración de fenoles.
Por tanto, el proceso de coagulación es capaz de alcanzar una reducción de la carga orgánica suficiente para cumplir los límites máximos de vertido de DQO, pero únicamente es capaz de disminuir la concentración de fenoles totales hasta 18 mg l-1, valor notablemente superior al establecido por la legislación autonómica (2 mg l-1).
Proceso de Coagulación-Fenton
Con el objetivo de reducir la concentración de los derivados fenólicos en el efluente procedente del proceso de coagulación, un posterior sistema de oxidación Fenton fue implementado teniendo en cuenta su capacidad para eliminar esta clase de compuestos (Zazo et al., 2007).
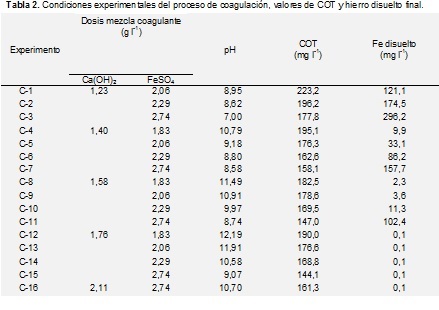
La concentración relativa de FeSO4 y Ca(OH)2 en la mezcla coagulante tiene una gran influencia en dos de los principales parámetros del posterior proceso Fenton: concentración de materia orgánica y hierro disuelto. Como concentraciones de partida de los coagulantes se utilizaron para el FeSO4 los valores optimizados en el proceso anterior de coagulación (2,29 g l-1) y la dosis teórica establecida por Degrèmont (2007) para el Ca(OH)2 (1,76 g l-1). Para alcanzar las mejores condiciones en el proceso Fenton, las dosis más óptimas de la mezcla coagulante serán aquellas que reduzcan la concentración de materia orgánica lo máximo posible, para disminuir las posteriores dosis requeridas de H2O2, y mantengan la mayor concentración posible en disolución de Fe2+. De acuerdo con estos criterios, las mezclas C-2, C-3 y C-7 de la Tabla 2 se seleccionaron para el proceso de oxidación.
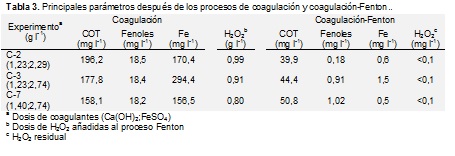
La Tabla 3 resume los principales parámetros después de los procesos de coagulanción y coagulación-Fenton de los experimentos C-2, C-3 y C-7. En todos ellos, COT fue significativamente menor que el límite de descarga. Sin embargo, la concentración de hierro y fenoles excedió sus respectivos valores umbrales de 10 y 2 mg l-1. El proceso de coagulación-Fenton alcanzó valores de COT de 39,9, 44,4 y 50,8 mg l-1 para C-2, C-3 y C-7, lo que se corresponde con eficiencias de eliminación superiores al 95%. El experimento con mayor contenido en hierro (C-3) tuvo una concentración de 1,5 mg l-1, notablemente inferior al límite de vertido. Por otro lado, con respecto a los fenoles, su concentración después del proceso de coagulación-Fenton se redujo hasta valores 0,18 mg l-1, considerablemente inferiores al valor máximo (2 mg l-1). Por tanto, teniendo en cuenta la reducción tanto de COT como de fenoles totales la mezcla coagulante C-2 se seleccionó para la optimización del proceso Fenton.
 Además del pH y la temperatura, los principales parámetros que afectan la eficacia del proceso Fenton son la concentración de H2O2 y el tiempo de reacción. Ambos han sido tenidos en cuenta en este trabajo. Primeramente, la concentración de peróxido de hidrogeno se optimizó debido a que su elevado coste supone una de las principales desventajas de este tratamiento (Esplugas et al., 2002). A pesar de que la concentración inicial de H2O2 (entorno a 1 g l-1) gracias al proceso previo de coagulación es considerablemente baja en comparación con otros estudios (Peres et al., 2003; San Sebastián et al., 2004), se trató de disminuir su dosis aún más. La Figura 1 muestra la evolución del COT (círculos negros) y de los fenoles totales (círculos blancos) usando diferentes dosis de H2O2. Una significativa reducción del COT se observa hasta dosis de 3 g l-1, a partir de la cual el incremento en la concentración de peróxido de hidrogeno produce un menor efecto en la eliminación de la materia orgánica. Este hecho previamente descrito por Bautista et al., 2007 es consecuencia al efecto “scavenger”. Por su parte, la concentración de fenoles se reduce hasta 0,09 g l-1 para dosis de 2 g l-1, aunque el límite máximo de vertido (2 mg l-1) es alcanzado usando 0,30 g l-1 de peróxido de hidrógeno.
Además del pH y la temperatura, los principales parámetros que afectan la eficacia del proceso Fenton son la concentración de H2O2 y el tiempo de reacción. Ambos han sido tenidos en cuenta en este trabajo. Primeramente, la concentración de peróxido de hidrogeno se optimizó debido a que su elevado coste supone una de las principales desventajas de este tratamiento (Esplugas et al., 2002). A pesar de que la concentración inicial de H2O2 (entorno a 1 g l-1) gracias al proceso previo de coagulación es considerablemente baja en comparación con otros estudios (Peres et al., 2003; San Sebastián et al., 2004), se trató de disminuir su dosis aún más. La Figura 1 muestra la evolución del COT (círculos negros) y de los fenoles totales (círculos blancos) usando diferentes dosis de H2O2. Una significativa reducción del COT se observa hasta dosis de 3 g l-1, a partir de la cual el incremento en la concentración de peróxido de hidrogeno produce un menor efecto en la eliminación de la materia orgánica. Este hecho previamente descrito por Bautista et al., 2007 es consecuencia al efecto “scavenger”. Por su parte, la concentración de fenoles se reduce hasta 0,09 g l-1 para dosis de 2 g l-1, aunque el límite máximo de vertido (2 mg l-1) es alcanzado usando 0,30 g l-1 de peróxido de hidrógeno.
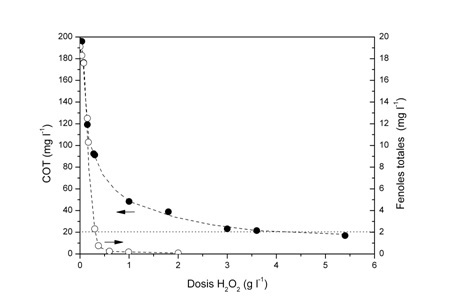 Figura 1. Influencia de la dosis de H2O2 en el COT (●) y en la concentración de fenoles totales (○).
Figura 1. Influencia de la dosis de H2O2 en el COT (●) y en la concentración de fenoles totales (○).
Posteriormente el tiempo de reacción fue optimizado para la dosis óptima de H2O2 (0,30 g l-1). El proceso alcanzó las máximas eficacias de eliminación tanto de COT como fenoles en los primeros 15 minutos de reacción.
Ecotoxicidad y biodegradabilidad
La Figura 2 muestra la relación entre la inhibición de la luminiscencia de la bacteria V. fischeri y el porcentaje de dilución del agua tanto bruta como tratada por los procesos de coagulación (C-7) y de coagulación-Fenton.
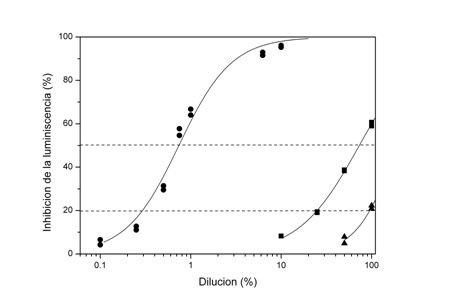 Figura 2. Curva de inhibición-dilución del efluente residual bruta (●), agua trata por el proceso de coagulación (■) y por el proceso de coagulación-Fenton (▲).
Figura 2. Curva de inhibición-dilución del efluente residual bruta (●), agua trata por el proceso de coagulación (■) y por el proceso de coagulación-Fenton (▲).
El efluente previo al tratamiento mostro ser altamente tóxico (200 Equitox m-3) y no biodegradable (DBO5/DQO=0,003). Ambos tratamiento consiguen disminuir notablemente la ecotoxidad del agua e incrementar su biodegradabilidad. Después del proceso de coagulación se obtienen aguas con valores de ecotoxicidad de 1,9 Equitox m-3, inferiores a los establecidos por la legislación (25 Equitox m-3), pero escasamente biodegradables (DBO5/DQO=0,03). El proceso integrado de coagulación-Fenton no sólo reduce muy significativamente la ecotoxicidad del agua residual bruta sino que incrementa su biodegradabilidad hasta 0,37 (ratio DBO5/DQO), valor cercano al que considera al agua como biodegradable (0,4-0,6) (Al-Momani et al., 2002).
Conclusiones
El proceso integrado de coagulación-Fenton resulto ser un tratamiento adecuado para tratar efluentes de la industria de cosméticos. Un primer proceso de coagulación con dosis de 2,29 y 1,23 g l-1 de FeSO4 y Ca(OH)2, respectivamente, alcanza reducciones notables de materia orgánica (>83%) pero insignificantes de derivados fenólicos. La integración de un posterior proceso Fenton, con dosis de H2O2 de 0,30 g l-1 y tiempos de reacción de 15 minutos, permite no sólo la muy significativa reducción de la materia orgánica (>96%) sino la disminución de la concentración de fenoles totales hasta valores considerablemente inferiores a los límites de vertido (0,18 mg l-1), reduciendo la ecotoxicidad e incrementando la biodegradabilidad del agua tratada.
Referencias
Al-Momani, F., Touraud, E., Degorce-Dumas, J.R., Roussy, J., Thomas, O. (2002) Biodegradability enhancement of textile dyes and textile wastewater by VUV photolysis. J. Photoch. Photobio. A. 153, 191-197.
Bautista, P., Mohedano, A.F., Gilarranz, M.A., Casas, J.A., Rodríguez, J.J. (2007) Application of Fenton oxidation to cosmetic wastewaters treatment. J. Hazard. Mat. 143, 28-134.
Degrèmont (2007) Water Treatment Handbook, 7th Ed., Lavousier Wiley, New York.
Esplugas, E., Giménez, J., Contreras, S., Pascual, E., Rodríguez, M. (2002) Comparison of different advanced oxidation processes for phenol degradation. Water Res. 36, 1034-1042.
Lin, S.H., Lin, C.M., Leu, H.G. (1999) Operating characteristics and kinetic studies of wastewater treatment by Fenton oxidation. Water Res. 33, 1735-1741.
Perdigón-Melón, J.A., Carbajo, J.B., Petre, A.L., Rosal, R., Garcia-Calvo, E. (2010) Coagulation-Fenton coupled treatment for ecotoxicity reduction in highly polluted industrial wastewater. J. Hazard. Mat. 181, 127-132.
Peres, J.A., Beltrán de Heredia, J., Domínguez, J.R., (2004) Integrated Fenton’s reagent-coagulation/flocculation process for the treatment of cork processing wastewaters J. Hazard. Mat. 107, 115-121.
San Sebastián, N., Fíguls, J., Font, X., Sánchez, A. (2003) Pre-oxidation of an extremely polluted industrial wastewater by the Fenton´s reagent. J. Hazard. Mater. 101, 315-322.
Tomaszewska, M., Mozia, S., Morawski, A.W. (2004) Removal of organic matter by coagulation enhanced with adsorption on PAC. Desalination 161, 79-87.
Zazo, J.A., Casas, J.A., Molina, C.B., Quintanilla, A., Rodríguez, J.J. (2007) Evolution of ecotoxicity upon Fenton´s oxidation of phenol in water. Environ. Sci. Technol. 41, 7164-7170.

Tenemos una planta de aguas residuales en una empresa Teñidora de Textiles.
El manejo de los tintes en las aguas servidas hacia el rió ha sido una lucha casi perdida.
Como me pueden orientar
ccomo hago para suscribierme al feed? no me abre bien el enlace