![]()
pH del Suelo y Nutrición Vegetal
En un post anterior, hablamos de la importancia del pH del suelo desde diversos puntos de vista. Hoy abundaremos sobre su importancia en la nutrición vegetal, es decir en la asimilación de los nutrientes por las plantas. De nuevo, se trata de un post destinado a los estudiantes, que no será de interés para los profesionales, que deben dirigirse a los post al respecto de Salvador González Carcedo.

Compost: Fertilizante Orgánico
En los ecosistemas naturales, los elementos químicos esenciales que las plantas absorben de las soluciones del suelo para nutrirse, son reincorporados al medio edáfico cuando sus restos muertos (necromasa) se descomponen en ese gran reactor metabólico que resulta ser el suelo. Sin embargo, en los agroecosistemas la dinámica natural del medio edáfico se encuentra muy perturbada debido a la extracción de biomasa (y de sus elementos minerales asociados), las labores agrícolas, la adicción de fertilizantes, etc. Del mismo modo, los pesticidas deterioran las comunidades edáficas naturales y su potencial para mineralizar y humificar la necromasa. Si los nutrientes extraídos con la biomasa no son restaurados, el suelo se empobrece y pierde gran parte de su fertilidad, por lo que la producción agrícola y pastoral se ven seriamente amenazadas.
El crecimiento vegetal depende de diversos factores limitantes, tales como lo son el agua, la luz solar y numerosos elementos químicos esenciales para el desarrollo de las plantas. Entre estos últimos destacan el nitrógeno, fósforo y potasio. Por tanto, con vistas a mantener la productividad de los suelos agrícolas se añaden periódicamente productos químicos solubles en agua, es decir los fertilizantes, que restauren los extraídos al cosechar los cultivos. Como es lógico, los fertilizantes más habituales son denominados “NPK” (abreviaciones de los tres elementos previamente aludidos). Estas enmiendas inorgánicas actúan con mayor rapidez, pero su acción es breve comparada con las de las orgánicas.
En la etiqueta de un fertilizante inorgánico, por ejemplo, 10, 20, 20, indica las concentraciones relativas de nitrógeno, fósforo y potasio respectivamente. A los fertilizantes orgánicos solemos denominarlos abonos, siendo frecuente las enmiendas en base a estiércol de diferentes especies de ganado, residuos de cultivos, harina de huesos, materia compostada, etc. Estos últimos son mucho más complejos y variables que los inorgánicos en lo que respecta a su composición, aunque como hemos señalado su acción es lenta y temporalmente prolongada. Tienen adicionalmente la ventaja de restaurar la perdida de carbono orgánico y la estructura del suelo, lo cual mejora de paso las propiedades físicas del medio edáfico.
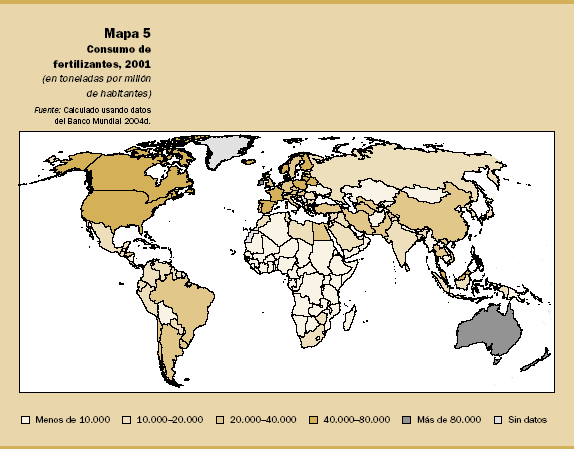
Consumo de fertilizantes en el mundo
El pH de las soluciones del suelo, en su área de contacto con las raíces, es decir, la rizosfera, repercute sobre la nutrición vegetal de varias maneras, entre las que cabría destacar:
El pH puede afectar la disponibilidad de los nutrientes en distinto grado y forma. Simplificando mucho, podemos decir que los sistemas radiculares de los vegetales absorben los nutrientes que se encuentras disueltos en el agua del suelo. Valores extremos de pH, ya por acidez, exceso de calcio o alcalinidad, pueden provocar la precipitación de ciertos elementos químicos con lo que permanecen en forma no disponible para las plantas. Cuando se trata de nutrientes esenciales, resulta obvio señalar que la especie vegetal padecerá problemas para alimentarse, por lo que se afectará negativamente a su desarrollo y producción. En el caso de los cultivos tal hecho puede arruinar las cosechas, si no se adoptan medidas correctoras.

Del mismo modo, el pH también puede repercutir en el proceso fisiológico de la absorción de los nutrientes por parte de las raíces. Todas las especies vegetales presentan unos rangos característicos de pH entre los cuales su absorción resulta óptima. Fuera de tales umbrales, la absorción radicular se ve entorpecida. Cuando los valores del pH se desvían en demasía de su óptimo, el sistema radicular puede deteriorarse o generarse toxicidad en la planta, debido a una asimilación excesiva de elementos químicos dañinos (fitotóxicos), como ocurre con el aluminio a pH muy ácidos.
Como ya mentamos en el post anterior, los medios áridos y semiáridos, en los que además abundan los suelos ricos en bases y/o salinos y las aguas de riego con pH superiores a 7.5, no debe extrañar que la asimilación de los nutrientes cuya solubilidad se ve afectada por tales ambientes iónicos (nutrientes como fósforo, hierro y manganeso) no sea la idónea para la producción de muchos cultivos. De hecho, la clorosis férrica es considerada como un grave problema en muchas regiones del mundo. Por tanto, se requiere ajustar el pH del suelo hacia valores adecuados, con vistas a corregir estados carenciales de fósforo, hierro y manganeso, es decir nutricionales.
Existe una gran variedad de factores que afectan al pH de la solución del suelo, siendo uno de los más importantes la relación o razón de absorción de nutrientes cargados negativamente (aniones) y positivamente (cationes). En general, un exceso de en la absorción de cationes sobre aniones, genera un descenso del pH, mientras que en el caso opuesto se induce su incremento. Mostremos el caso de un nutriente vital y necesario en dosis considerables para la producción de los cultivos, como es el nitrógeno.
El nitrógeno, puede ser aportado a la planta como catión amonio (NH4+) o como anión nitrato (NO3-). Resulta que la relación existente entre estas dos formas nitrogenadas en la solución de nutrientes puede cambiar de formas opuestas el pH previo a la enmienda. Las raíces modifican con facilidad el ambiente iónico (pH) en su rizosfera colindante con vistas a poder incrementar su potencial para la captación de los nutrientes, aumentando su “biodisponibilidad”. Cuando la planta absorbe preferentemente cationes (NH4+), se induce un exceso de carga negativa que la propia planta intenta neutralizar segregando cationes hidrógeno (H+), con lo que el pH de la solución desciende. Inversamente, sí se absorben preferentemente aniones (NO3-), las raíces liberan iones hidroxilo (OH-) o iones bicarbonato (HCO3-), intentando mantener la neutralidad eléctrica en la superficie de la raíz, con lo que el pH de la solución tiende a incrementarse. Cuando que las cantidades de amonio asimilados por la planta superan un cierto umbral puede resultar tóxico, generando a la par interacciones, a veces no deseadas, con otros cationes (como por ejemplo, calcio, potasio y magnesio). Por tanto, un adecuado balance en la relación NH4+/NO3- puede resultar esencial para sostener una adecuada nutrición vegetal.
Del mismo modo, el hierro, que es el elemento esencial cuya solubilidad es muy sensible respecto al pH y sus cambios, a menos que se realicen enmiendas del mismo en forma de quelatos. Su biodisponibilidad para la planta resulta ser generalmente menor del 50% por encima de pH 7, mientras que a pH 8 no puede ser asimilado, por cuanto precipita en forma de hidróxido férrico Fe(OH)3. Por el contrario, por debajo de pH 6.5, más del 90% de este elemento permanece disuelto y disponible para ser absorbido por los sistemas radiculares de las plantas. El manganeso sigue una dinámica similar al hierro.
Por tanto, podemos concluir que entre los valores de pH del suelo de 5.0-6.5, la mayor parte de los nutrientes suelen estar en forma de especies químicas directamente asimilables para la mayor parte de los vegetales. Sin embargo, cuando se exceden los valores de pH 6.5, la formación de precipitados puede causar importantes problemas de nutrición vegetal, mientras que para pH inferiores a 5 el sistema radicular corre graves riesgos de ser dañado.
Continuara……
Juan José Ibáñez

esta muy interesante su documento lo revise y me sirvio de mucho ya que esta muy explicado y resumida gracias por compartir su tiempo y conocimientos.
quisiera que me hablaras un poco de los nutrientes esenciales de las plantas (N, P, K, Mg)en especial de este ultimo.
muy bueno para mis tareas
gracias
Por favor ayúdeme, cómo puedo realizar los cálculos de necesidades de carbonato de calcio en el suelo; por ej. de un suelo con ph 5 a 6,5
mira lo encuentro super interesante pero necesito una respuesta para esta pregunta
los fertilizantes como afectan al ph en el suelo
es re urgente ia q soy un estudiante
grasias
Gracias por sus comentarios, los cuales me resultan muy útiles.
Por otra parte necesito ayuda acerca de si puedo utilizar ácido fosfórico como fuente de fosforo en cultivo de tomate. Gracias.
MUY INTERESANTE , ADICIONALMENTE , ME DIO TRANQUILIDAD EL VER QUE LO QUE ME ESTA PASANDO EN MI CULTIVO DE ROSAS Y QUE LAS PRECAUCIONES QUE HE TOMADO SON LAS CORRECTAS , PERO CUAL PUEDE SER LA RELACION CORRECTA EN LO QUE A NITROGENO CORESPODE ENTRE NITRICA Y AMONIACAL EN UNA FERTILIZACIÒN NORMAL , AGRADECERÌA SU COMENTARIO PUES TENÌA UN SUELO ALCALINO Y AHORA LUCHO POR INCREMENTAR EL PH , NO HE PUESTO ACIDO FUERTES A EL SUELO ,USO ACIDO CITRICO PARA ESTE EFECTO PERO YA UN AÑO QUE NO PONGO EN MI FERTILIZACIÒN NINGUN ACIDIFICANTE
La informacion que ustedes dan es muy interesante, de gran ayuda para poder continuar desarrollandome profesionalmente.
Gracias a usted puedo completar mi proyecto de ciencias. felicidades!!!
muy importante todo su comentario sobre nutricion,espero que me hables sobre el silicio como nutriente y como desbloqueador de elementos pesados en el suelo.como el aluminio,hierro y manganeso.
Estuvo muy interesante y científico lo del ph y su relación con el ambiente edáfico junto a las plantas.. Me agradaría que se profundice, acerca de la nutrición vegetal con fertilizantes orgánicos e inorgánicos, cuales son las ventajas y desventajas de los dos métodos… Y sobre todo como hago para que el primer método (fertilizante orgánico) funcione igual de rápido como lo hacen los inorgánicos referente al modo o velocidad de acción.
este correo es para es para la tarea de ciencias
Muy importante este tema me gustaria de ser posible me hable sobre los efectos y formas de bloqueo que tienen los microelementos al no estar disponible para las plantas
Gracias
Me gustaría que me pudiera comentar cómo puedo realizar los cálculos de necesidades de carbonato de calcio que se necesitan para cambiar un ph de 5 a uno de 6 considerando un terreno con una capa arable de 12 cm. y una densidad aparente de 1.33
gracias.!!!
Tengo una compostera, en donde proceso cerca de 300 ton. mensuales de abono organico mineral. Es una mezcla compleja de estiecoles de porcinos, bovinos, aves, carbonatos, sulfatos, fosfatos. El proceso de fermentación aerobia dura de 50 a 60 días.El pH final es 8; siendo una enmienda organico- mineral que opina usted, solicito algunas recomendaciones extras. Gracias….
solo quiero saber que es la nutricion vegetal, los nutrientes de las plantas, la raiz, el tallo como sistema conductor de la planta, la hoja es una estructura conductor, transporte de nutrientes. ¿que es? todo eso mas nada no quiero saber nada de eso que dice ahi!! porfavor ayudenme de alguna manera porfa es urgente este tema chao esperando que me ayuden Bya: Valeskita
estoy manejando una empresa de nutrición de jardín espero que puedan informarme de sus experimentos