![]()
La investigación sobre simbiosis en leguminosas y su aplicación en Medicina
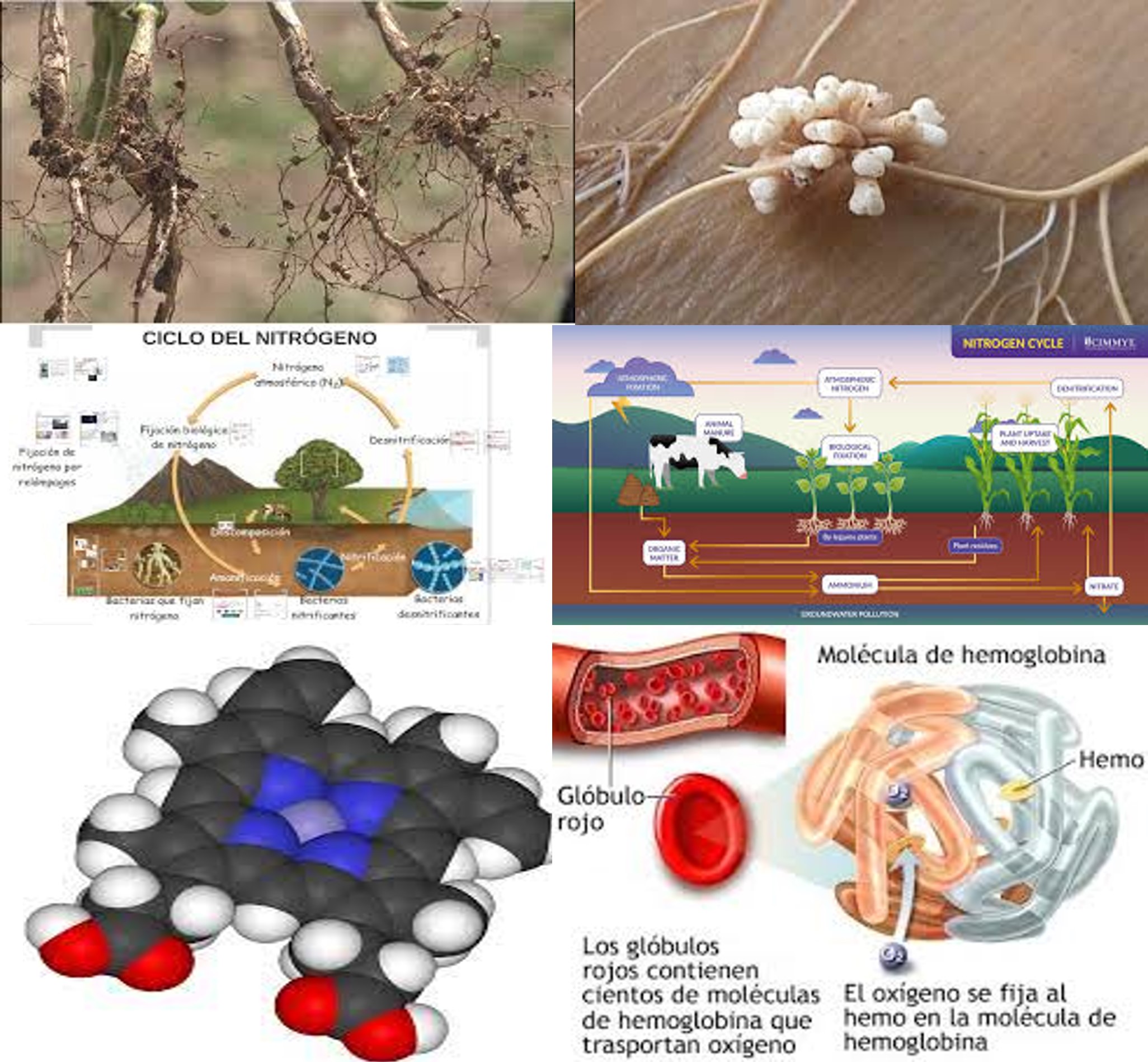
Fuente: Colaje imágenes Google
Grupo Hemo, simbiosis, Rhizobium, fijación del nitrógeno y leguminosas. Sobre todos estos asuntos versa la nota de prensa que os mostramos hoy. Se trata de un tema propio de la bitácora, pero también es uno de los que menos domino dada mi formación académica y actividad investigadora. Por lo tanto, no añadiré comentario alguno sobre esta investigación, salvo, una breve entradilla que concierne a un aspecto que se me antoja interesante para lo edafólogos. En principio, todo apunta a que los investigadores analizaban simplemente los mecanismos de la fisiología de las relaciones entre leguminosas y bacterias del suelo fijadoras simbióticas de nitrógeno. Sin embargo, “al parecer”, toparon con una sorpresa cuyas implicaciones potenciales podrían ser de gran importancia en medicina. El estudio en sí mismo parece interesante, si los resultados terminan siendo corroborados, por supuesto. Conocer todo lo relacionado con la fijación biológica del nitrógeno resulta ser de vital importancia en agricultura, así como para una mejor comprensión del ciclo global del nitrógeno, del que tanto os hemos hablado.Según los autores: “»Este estudio demuestra que la investigación básica en las interacciones planta-microbio también tiene potencial para traducirse en aplicaciones terapéuticas«.
Como el mundo de la tecnociencia me parece bastante turbio, cabe esperar dos posibilidades: (a) que en el denominado “potencial” siempre va acompañado de los palabros “podría, o no podría”, tal vez los esperanzadores resultados que claman los autores no sean más que propaganda publicitaria o un canto de sirenas. Es decir, al añadir posibles aplicaciones por demostrar, resulta más fácil que la publicación sea aceptada por las revistas de prestigio en un mundo apabullado por la mentalidad tecnocientífica. Pero también cabe la posibilidad de (b) que efectivamente en el ámbito de la agronomía, fisiología de las plantas y el mundo de los suelos, la investigación básica, sin más da lugar a descubrimientos de importancia, que a posteriori, vía investigación traslacional, enriquezcan el arsenal de medicamentos que velan por la salud humana como ya lo fueran los antibióticos entre muchos otros ejemplos. ¿a o b?. ¡A saber! Obviamente ojalá fuera b, pero…… como mínimo habrá que esperar a que se demuestren tales potencialidades.
Y esta resulta ser la grandeza de la ciencia básica, que sus hallazgos, tarde o temprano, terminan siendo de gran utilidad en otros ámbitos del saber, entre los cuales algunos eran insospechados. Debemos impulsar la investigación básica en las ciencias del suelo desde esta perspectiva. No se trata de repetir ad nausean la importancia de los suelos conforme a las demandas y urgencias de la sociedad en un momento dado. El caso de los antibióticos fue paradigmático, pero hay muchos más y este es un ejemplo. Os dejo pues con la noticia, que seguro que interesará a los estudiosos de la edafomedicina y sus posibles aplicaciones en medicina……..
Juan José Ibáñez
Continúa…….
Científicos identifican una molécula de planta que absorbe hemo rico en hierro
por Anne Trafton para MIT News; Boston MA (SPX) 12 de agosto de 2022
Las relaciones simbióticas entre las legumbres y las bacterias que crecen en sus raíces son críticas para la supervivencia de las plantas. Sin esas bacterias, las plantas no tendrían fuente de nitrógeno, un elemento que es esencial para la construcción de proteínas y otras biomoléculas, y dependerían de los fertilizantes nitrogenados en el suelo.
Para establecer esa simbiosis, algunas plantas leguminosas producen cientos de péptidos que ayudan a las bacterias a vivir dentro de estructuras conocidas como nódulos dentro de sus raíces. Un nuevo estudio del MIT revela que uno de estos péptidos tiene una función inesperada: absorbe todo el hemo disponible, una molécula que contiene hierro. Esto envía a las bacterias a un modo de inanición de hierro que aumenta su producción de amoníaco, la forma de nitrógeno que es utilizable para las plantas.
«Este es el primero de los 700 péptidos en este sistema para el cual se ha elaborado un mecanismo molecular realmente detallado», dice Graham Walker, profesor de biología de la Sociedad Americana del Cáncer en el MIT, profesor del Instituto Médico Howard Hughes y autor principal del estudio.
Este péptido secuestrador de hemo podría tener usos beneficiosos en el tratamiento de una variedad de enfermedades humanas, dicen los investigadores. Eliminar el hemo libre de la sangre podría ayudar a tratar enfermedades causadas por bacterias o parásitos que necesitan hemo para sobrevivir, como P. gingivalis (enfermedad periodontal) o toxoplasmosis, o enfermedades como la enfermedad de células falciformes o la sepsis que liberan demasiado hemo en el torrente sanguíneo.
«Este estudio demuestra que la investigación básica en las interacciones planta-microbio también tiene potencial para traducirse en aplicaciones terapéuticas«, dice Siva Sankari, científica investigadora del MIT y autora principal del estudio, que aparece en Nature Microbiology.
Otros autores del artículo incluyen a Vignesh Babu, un científico investigador del MIT; Kevin Bian y Mary Andorfer, ambos postdoctorados del MIT; Areej Alhhazmi, ex becaria de KACST-MIT Ibn Khaldun Fellowship for Saudi Arabian Women; Kwan Yoon y Dante Avalos, estudiantes graduados del MIT; Tyler Smith, instructor de biología del MIT; Catherine Drennan, profesora de química y biología del MIT e investigadora del Instituto Médico Howard Hughes; Michael Yaffe, profesor de ciencias David H. Koch y miembro del Instituto Koch para la Investigación Integrativa del Cáncer del MIT; y Sebastián Lourido, profesor de Biología de Desarrollo Profesional de la Familia Latham en el MIT y miembro del Instituto Whitehead para la Investigación Biomédica.
Control de hierro
Durante casi 40 años, el laboratorio de Walker ha estado estudiando la simbiosis entre las legumbres y los rizobios, un tipo de bacteria fijadora de nitrógeno. Estas bacterias convierten el gas nitrógeno en amoníaco, un paso crítico del ciclo del nitrógeno de la Tierra que hace que el elemento esté disponible para las plantas (y para los animales que comen las plantas).
La mayor parte del trabajo de Walker se ha centrado en una planta similar al trébol llamada Medicago truncatula. Las bacterias fijadoras de nitrógeno provocan la formación de nódulos en las raíces de estas plantas y, finalmente, terminan dentro de las células vegetales, donde se convierten a su forma simbiótica llamada bacteroides.
Hace varios años, los biólogos de plantas descubrieron que Medicago truncatula produce alrededor de 700 péptidos que contribuyen a la formación de estos bacteroides. Estos péptidos se generan en ondas que ayudan a las bacterias a hacer la transición de vivir libremente a incrustarse en las células vegetales donde actúan como máquinas fijadoras de nitrógeno.
Walker y sus estudiantes eligieron uno de estos péptidos, conocido como NCR247, para profundizar más profundamente. Los estudios iniciales revelaron que cuando las bacterias fijadoras de nitrógeno fueron expuestas a este péptido, el 15 por ciento de sus genes se vieron afectados. Muchos de los genes que se volvieron más activos estaban involucrados en la importación de hierro.
Luego, los investigadores descubrieron que cuando fusionaron NCR247 con una proteína más grande, la proteína híbrida era inesperadamente de color rojizo. Esta observación fortuita condujo al descubrimiento de que NCR247 se une al hemo, una molécula orgánica que contiene hierro en forma de anillo que es un componente importante de la hemoglobina, la proteína que los glóbulos rojos utilizan para transportar oxígeno.
Estudios posteriores revelaron que cuando NCR247 se libera en las células bacterianas, secuestra la mayor parte del hemo en la célula, enviando a las células a un modo de inanición de hierro que las hace comenzar a importar más hierro del entorno externo.
«Por lo general, las bacterias afinan su metabolismo del hierro, y no absorben más hierro cuando ya hay suficiente«, dice Sankari. «Lo bueno de este péptido es que anula ese mecanismo e indirectamente regula el contenido de hierro de las bacterias».
La nitrogenasa, la principal enzima que las bacterias usan para fijar el nitrógeno, requiere de 24 a 32 átomos de hierro por molécula de enzima, por lo que la afluencia de hierro adicional probablemente ayude a esas enzimas a ser más activas, dicen los investigadores. Esta afluencia está programada para coincidir con la fijación de nitrógeno, encontraron.
«Estos péptidos se producen en una onda en los nódulos, y la producción de este péptido en particular es mayor cuando las bacterias se preparan para fijar nitrógeno. Si este péptido se secretara durante todo el proceso, entonces la célula tendría demasiado hierro todo el tiempo, lo cual es malo para la célula», dice Sankari.
Sin el péptido NCR247, Medicago truncatula y rhizobium no pueden formar una simbiosis fijadora de nitrógeno efectiva, mostraron los investigadores.
«Muchas direcciones posibles»
El péptido que los investigadores estudiaron en este trabajo puede tener usos terapéuticos potenciales. Cuando el hemo se incorpora a la hemoglobina, realiza una función crítica en el cuerpo, pero cuando está suelto en el torrente sanguíneo, puede matar las células y promover la inflamación. El hemo libre puede acumularse en la sangre almacenada, por lo que tener una forma de filtrar el hemo antes de que la sangre se transfunda en un paciente podría ser potencialmente útil.
Una variedad de enfermedades humanas conducen a hemo libre que circula en el torrente sanguíneo, incluida la anemia de células falciformes, la sepsis y la malaria. Además, algunos parásitos y bacterias infecciosas dependen del hemo para su supervivencia, pero no pueden producirlo, por lo que lo eliminan de su entorno. El tratamiento de tales infecciones con una proteína que absorbe todo el hemo disponible podría ayudar a evitar que las células parásitas o bacterianas puedan crecer y reproducirse.
En este estudio, Lourido y los miembros de su laboratorio demostraron que el tratamiento del parásito Toxoplasma gondii con NCR427 evitó que el parásito formara placas en las células humanas.
Los investigadores ahora están buscando colaboraciones con otros laboratorios en el MIT para explorar algunas de estas aplicaciones potenciales, con fondos de una beca de investigación del profesor Amar G. Bose.
«Hay muchas direcciones posibles, pero todas están en una etapa muy temprana», dice Walker. «El número de aplicaciones clínicas potenciales es muy amplio. Puedes hacer más de una apuesta en este juego, lo cual es algo intrigante».
Actualmente, la proteína humana hemopexina, que también se une al hemo, se está explorando como un posible tratamiento para la anemia de células falciformes. El péptido NCR247 podría proporcionar una alternativa más fácil de implementar, dicen los investigadores, porque es mucho más pequeño y podría ser más fácil de fabricar y entregar en el cuerpo.
La investigación fue financiada en parte por el Centro de Ciencias de la Salud Ambiental del MIT, la Fundación Nacional de Ciencias y los Institutos Nacionales de Salud.
Informe de investigación: «Un péptido vegetal secuestrador de hemo promueve la absorción de hierro en bacterias simbióticas»
