![]()
Fijación del Nitrógeno por los suelos: una resiliencia inesperada
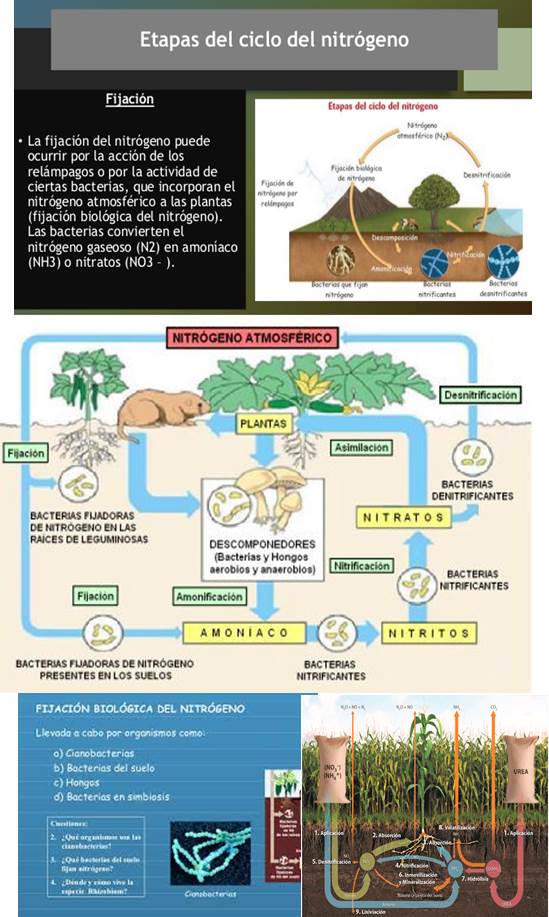
Cuatro perspectivas del ciclo del Nitrógeno. Fuente. Imágenes Google
Los nutrientes en el suelo deben encontrarse en forma biodisponible para poder ser asimilados por las plantas. Por su parte el nitrógeno resulta ser un elemento abundantísimo en la atmósfera, aunque no en un estado biodisponible. Por ello, la vida a necesitado desarrollar un complejo entramado de reacciones bioquímicas con vistas a la alcanzar la fijación del nitrógeno vía enzimática. Hablamos de la nitrogenasa en el sentido más amplio del término. Hasta la fecha, según la nota de prensa, en el conjunto de procesos, es decir la cadena de reacciones inherentes, era necesario el molibdeno, un elemento traza que en los suelos es muy escaso, y a veces, insuficiente. Sin embargo, con el tiempo, se ha visto que otros metales como el hierro y el vanadio daban lugar a otras “nitrogenasas alternativas”. Es decir, que si en un territorio el molibdeno es alarmantemente escaso, puede alcanzarse la biodisponibilidad del nitrógeno vía “alternativa”, haciendo uso del vanadio y quizás el hierro. De la nota de prensa que os presentamos hoy se desprende que ¡la intervención de este último metal!, parece haber sido descubierta por los autores. Sin embargo si utilizáis vuestro motor de búsqueda, observaréis que no es “exactamente” así. Con toda la sinceridad y humildad del mundo, mis conocimientos sobre fisiología vegetal se fugaron junto a algún grupo de neuronas que he perdido a lo largo del sendero de mi vida. ¡Lo lamento!. Empero a pesar de todo he traducido la nota de prensa original y añadido algún material (demasiado técnico para esta bitácora) elaborado por la Estación Experimental del Zaidín –EEZ-(CSIC) en el que enlazo algunos vocablos con otras páginas Web, más divulgativas. No voy pues hoy a relatar nada que no sea mi impresión personal, ya que el resto lo podéis leer abajo.
No me cansa llamar la atención sobre la cantidad de “emprendimiento” que atesora la naturaleza cuando debe sortear obstáculos que impiden su pleno asentamiento en la biosfera, o en algún espacio geográfico de la misma. Según la noticia, el molibdeno escasea en ciertos suelos y, según los autores, como mínimo en los ecosistemas boreales. Y es allí en donde dicen que esa nitrogenasa alternativa, con vanadio reemplaza total o parcialmente su función ecosistémica. Aunque al parecer, repito, que al parecer, al menos existe otra posibilidad, el hierro.
Rescatamos estas frase de la nota de prensa traducida aquí al español-castellano: “Investigadores de la Universidad de Princeton descubrieron que la naturaleza ha desarrollado un método de respaldo/alternativo para convertir el nitrógeno atmosférico en la forma de nutrientes asimilables para el crecimiento de las plantas y la fertilidad del suelo. Los investigadores informan que el proceso conocido como fijación de nitrógeno puede ser llevado a cabo por el metal vanadio en los ecosistemas, particularmente en el hemisferio norte, donde el catalizador primario de molibdeno es escaso. El estudio sugiere que la capacidad de la naturaleza para restaurar los ecosistemas a raíz de las perturbaciones causadas por el hombre o fertilizar las tierras agrícolas es más resistente de lo que se pensaba. Aunque el nitrógeno es esencial para todos los organismos vivos (constituye el 3% del cuerpo humano) y comprende el 78% de la atmósfera de la Tierra, es sumamente difícil para las plantas y los sistemas naturales el acceso al mismo. El nitrógeno atmosférico no es directamente utilizable por la mayoría de los seres vivos. En la naturaleza, los microbios especializados en suelos y cuerpos de agua convierten el nitrógeno en amoníaco, una forma crucial de nitrógeno a la que la vida puede acceder fácilmente, a través de un proceso llamado fijación de nitrógeno. En la agricultura, la soja y otras leguminosas que facilitan la fijación de nitrógeno se pueden sembrar para restaurar la fertilidad del suelo”.
Desde otro punto de vista, me llama la atención a la incorporación que hacen de las emisiones antropogénicas con las que el ser humano ha cargado la atmósfera y que como no también transporta vanadio y molibdeno, incorporándolas con toda naturalidad a la dinámica de los ecosistemas y el ciclo del nitrógeno. ¡No critico tal acción, por cuanto querámoslo o no, allí se encuentran ahora. Simplemente y sin apenas percatarnos evoluciona nuestro pensamiento conforme se consolida nuestra Tecno-biosfera. Así mismo, los investigadores que han realizado este estudio nos informan de que: “Una consecuencia de este hallazgo es que las estimaciones actuales de la cantidad de entrada de nitrógeno en los bosques boreales a través de la fijación pueden haber sido subestimadas significativamente. Este es un problema importante para nuestra comprensión de los requerimientos de nutrientes para los ecosistemas forestales”.
Por su parte la Página Web de la EEZ, señala una posible aplicación práctica: “Una vez descifrada la química de la fijación se podría abrir la posibilidad de un proceso industrial alternativo al de Haber Bosch para la obtención de fertilizante nitrogenado. Sería interesante, pues el funcionamiento del sistema Haber Bosch, que produce unos 80 MTn. año de amonio, supone el 1 % del total de la energía consumida a nivel mundial”.
Si cabe reprochar la apelación a que el papel del molibdeno y vanadio no es recogido por los modelos actuales climáticos. ¡Menuda estupidez!. Si tuviéramos que incorporar a estos modelitos todos los elementos, interacciones y procesos que los científicos desean, no podríamos resolver problemas, modelizar, simular, laborar algoritmos, y bla, bla, bla, ni mediante la computación cuántica que tanto ansiamos.
Todo el post constata hasta qué punto la vida trabaja e innova con tal de otorgar a los suelos la fertilidad que necesitan para el mantenimiento de los ecosistemas, a lo cual hay que incluir ahora nuestras contaminaciones.
Juan José Ibáñez
Continúa…………
Researchers find nature’s backup plan for converting nitrogen into plant nutrients
by Staff Writers; Princeton NJ (SPX) Nov 12, 2019
Although nitrogen is essential for all living organisms – it makes up 3% of the human body – and comprises 78% of Earth’s atmosphere, it’s almost ironically difficult for plants and natural systems to access it.
Atmospheric nitrogen is not directly usable by most living things. In nature, specialized microbes in soils and bodies of water convert nitrogen into ammonia – a crucial form of nitrogen that life can easily access – through a process called nitrogen fixation. In agriculture, soybeans and other legumes that facilitate nitrogen fixation can be planted to restore soil fertility. Los investigadores encuentran el plan de respaldo de la naturaleza para convertir el nitrógeno en nutrientes para las plantas
An additional obstacle in the process of making nitrogen available to the plants and ecosystems that rely on it is that microbial nitrogen «fixers» incorporate a complex protein called nitrogenase that contains a metal-rich core. Existing research has focused on nitrogenases containing a specific metal, molybdenum.
The extremely small amount of molybdenum found in soil, however, has raised concerns about the natural limits of nitrogen fixation on land. Scientists have wondered what restrictions the scarcity of molybdenum places on nature’s capacity to restore ecosystem fertility in the wake of human-made disturbances, or as people increasingly search for arable land to feed a growing population.
Princeton University researchers have found evidence that other metals can facilitate nitrogen fixation when molybdenum is scarce, which suggests that the process may be more resilient than previously thought, according to a study published in the journal Proceedings of the National Academy of Sciences. Working in a 372 mile (600 kilometer) stretch of boreal forest in Canada, the researchers found that nitrogen fixation at an ecosystem scale can also be catalyzed by the metal vanadium, particularly in northern regions with limited natural nitrogen inputs.
Los investigadores encuentran el plan de respaldo de la naturaleza para convertir el nitrógeno en nutrientes para las plantas
Por escritores del personal; Princeton NJ (SPX) 12 de noviembre de 2019
Investigadores de la Universidad de Princeton descubrieron que la naturaleza ha desarrollado un método de respaldo para convertir el nitrógeno atmosférico en la forma de nutrientes crítica para el crecimiento de las plantas y la fertilidad del suelo. Los investigadores informan que el proceso conocido como fijación de nitrógeno puede ser llevado a cabo por el metal vanadio en los ecosistemas, particularmente en el hemisferio norte, donde el catalizador primario de molibdeno es escaso. El estudio sugiere que la capacidad de la naturaleza para restaurar los ecosistemas a raíz de las perturbaciones causadas por el hombre o fertilizar las tierras agrícolas es más resistente de lo que se pensaba.
Aunque el nitrógeno es esencial para todos los organismos vivos (constituye el 3% del cuerpo humano) y comprende el 78% de la atmósfera de la Tierra, es sumamente difícil para las plantas y los sistemas naturales el acceso al mismo.
El nitrógeno atmosférico no es directamente utilizable por la mayoría de los seres vivos. En la naturaleza, los microbios especializados en suelos y cuerpos de agua convierten el nitrógeno en amoníaco, una forma crucial de nitrógeno a la que la vida puede acceder fácilmente, a través de un proceso llamado fijación de nitrógeno. En la agricultura, la soja y otras leguminosas que facilitan la fijación de nitrógeno se pueden plantar para restaurar la fertilidad del suelo.
«This work prompts a major revision of our understanding of how micronutrients control ecosystem nitrogen status and fertility,» said senior author Xinning Zhang, assistant professor of geosciences and the Princeton Environmental Institute.
«We need to know more about how nitrogen fixation manifests in terms of nutrient budgets, cycling and biodiversity,» she said. «One consequence of this finding is that current estimates of the amount of nitrogen input into boreal forests through fixation may be significantly underestimated. This is a major issue for our understanding of nutrient requirements for forest ecosystems, which currently function as an important sink for anthropogenic carbon.»
Un obstáculo adicional en el proceso de hacer que el nitrógeno esté disponible para las plantas y los ecosistemas que dependen de él es que los «fijadores» de nitrógeno microbiano incorporan una proteína compleja llamada nitrogenasa que contiene un núcleo rico en metales. La investigación existente se ha centrado en las nitrogenasas que contienen un metal específico, el molibdeno.
Sin embargo, la cantidad extremadamente pequeña de molibdeno que se encuentra en el suelo ha generado preocupaciones sobre los límites naturales de la fijación de nitrógeno en la tierra. Los científicos se han preguntado qué restricciones impone la escasez de molibdeno a la capacidad de la naturaleza con vistas a restaurar la fertilidad del ecosistema tras las perturbaciones causadas por el hombre, o cuando las personas buscan cada vez más tierras cultivables para alimentar a una población en crecimiento.
Investigadores de la Universidad de Princeton han encontrado evidencia de que otros metales pueden facilitar la fijación de nitrógeno cuando el molibdeno es escaso, lo que sugiere que el proceso puede ser más resistente de lo que se pensaba, según un estudio publicado en la revista Proceedings of the National Academy of Sciences. Trabajando en una parcela de bosque boreal de 372 millas (600 kilómetros) en Canadá, los investigadores descubrieron que la fijación de nitrógeno a escala de ecosistema también puede ser catalizada por el vanadio metálico, particularmente en las regiones del norte con entradas limitadas de nitrógeno natural.
«Este trabajo provocará una revisión importante de nuestra comprensión de cómo los micronutrientes controlan el estado y la fertilidad del nitrógeno del ecosistema«, dijo el autor principal Xinning Zhang, profesor asistente de geociencias y el Instituto Ambiental de Princeton.
«Necesitamos profundizar en el conocimiento de cómo se manifiesta la fijación de nitrógeno en términos de necesidades de nutrientes, sus ciclos, así como progresar en los estudios de biodiversidad», dijo. «Una consecuencia de este hallazgo es que las estimaciones actuales de la cantidad de entrada de nitrógeno en los bosques boreales a través de la fijación pueden haber sido subestimadas significativamente. Este es un problema importante para nuestra comprensión de los requerimientos de nutrientes para los ecosistemas forestales, que actualmente funcionan como un sumidero importante para los carbones de origen antrópico.»
First author Romain Darnajoux, a postdoctoral research associate in Zhang’s research group, explained that the findings validate a long-held hypothesis in the scientific community that different metal variants of nitrogenase exist so that organisms can cope with changes in metal availability. The researchers found that vanadium-based nitrogen fixation was only substantive when environmental molybdenum levels were low.
«It would seem that nature evolved backup methods to sustain ecosystem fertility when the environment is variable,» Darnajoux said. «Every nitrogen-cycle step involves an enzyme that requires particular trace metals to work. Molybdenum and iron are typically the focus of scientific study because they’re considered to be essential in the nitrogen fixing enzyme nitrogenase. However, a vanadium-based nitrogenase also exists, but nitrogen input by this enzyme has been unfortunately largely ignored.»
El primer autor, Romain Darnajoux, asociado de investigación posdoctoral en el grupo de investigación de Zhang, explicó que los hallazgos corroboran una hipótesis aceptada como validad durante mucho tiempo por parte de la comunidad científica que defiende la existencia de diferentes variantes metálicas de la nitrógenasa para que los organismos puedan hacer frente a los cambios en la disponibilidad de metales. Los investigadores encontraron que la fijación de nitrógeno a base de vanadio solo era sustantiva cuando los niveles ambientales de molibdeno eran bajos.
«Parece que la naturaleza desarrolló métodos de respaldo para mantener la fertilidad del ecosistema cuando el ambiente es variable«, dijo Darnajoux. «Cada paso del ciclo del nitrógeno involucra una enzima que requiere metales traza particulares en su funcionamiento. El molibdeno y el hierro son típicamente el foco del estudio científico porque se consideran esenciales en la enzima nitrogenasa indispensable en lo concerniente a la fijación de nitrógeno. Sin embargo, una nitrogenasa a base de vanadio también existe, pero desafortunadamente se ha ignorado en gran medida el aporte de nitrógeno llevado a cabo por esta enzima”.
Darnajoux and Zhang worked with Nicolas Magain and Franc?ois Lutzoni at Duke University and Marie Renaudin and Jean-Philippe Bellenger at the University of Sherbrooke in Quebec.
The researchers’ results suggest that the current estimates of nitrogen input into boreal forests through fixation are woefully low, which would underestimate the nitrogen demand for robust plant growth, Darnajoux said. Boreal forests help mitigate climate change by acting as a sink for anthropogenic carbon. Though these northern forests do not see as many human visitors as even the most lightly populated metropolis, human activities can still have major impacts on forest fertility through the atmospheric transport of air pollution loaded with nitrogen and metals such as molybdenum and vanadium.
Darnajoux y Zhang trabajaron con Nicolas Magain y François Lutzoni en la Universidad de Duke y Marie Renaudin y Jean-Philippe Bellenger en la Universidad de Sherbrooke en Quebec.
Los resultados de los investigadores sugieren que las estimaciones actuales de la entrada de nitrógeno en los bosques boreales a través de la fijación son lamentablemente bajas, lo que subestimaría la demanda de nitrógeno para el crecimiento robusto de las plantas, dijo Darnajoux. Los bosques boreales ayudan a mitigar el cambio climático al actuar como sumidero del carbono antropogénico. Aunque estos bosques del norte no reciben tantos visitantes humanos como las metrópolis más escasamente pobladas, las actividades antrópicas aún pueden tener un gran impacto en la fertilidad de los bosques a través del transporte atmosférico de la contaminación del aire cargada de nitrógeno y metales como el molibdeno y el vanadio.
«Human activities that substantially change air quality can have a far reaching influence on how even remote ecosystems function,» Zhang said. «The findings highlight the importance of air pollution in altering micronutrient and macronutrient dynamics. Because air is a global commons, the connection between metals and nitrogen cycling and air pollution has some interesting policy and management dimensions.»
The researchers findings could help in the development of more accurate climate models, which do not explicitly contain information on molybdenum or vanadium in simulations of the global flow of nitrogen through the land, ocean and atmosphere.
The importance of vanadium-driven nitrogen fixation extends to other high latitude regions, and most likely to temperate and tropical systems, Darnajoux and Zhang said. The threshold for the amount of molybdenum an ecosystem needs to activate or deactivate vanadium nitrogen fixation that they found in their study was remarkably similar to the molybdenum requirements of nitrogen fixation found for samples spanning diverse biomes.
The researchers will continue the search for vanadium-based nitrogen fixation in the northern latitudes. They’ve also turned their eyes toward areas closer to home, initiating studies of micro- and macronutrient dynamics in temperate forests in New Jersey, and they plan to expand their work to tropical systems.
«Las actividades humanas que cambian sustancialmente la calidad del aire pueden tener una influencia de largo alcance sobre cómo funcionan incluso los ecosistemas remotos«, dijo Zhang. «Los hallazgos resaltan la importancia de la contaminación del aire en la alteración de la dinámica de los micronutrientes y macronutrientes. Debido a que el aire es un bien común mundial, la conexión entre los ciclos de metales y nitrógeno y la contaminación del aire tiene algunas dimensiones interesantes en la gestión política de la naturaleza «.
Los hallazgos de los investigadores podrían ayudar en el desarrollo de modelos climáticos más precisos, que no contienen información explícita sobre molibdeno o vanadio en las simulaciones del flujo global de nitrógeno a través de la tierra, el océano y la atmósfera.
La importancia de la fijación de nitrógeno impulsado por vanadio se extiende a otras regiones de latitudes altas, y muy probablemente a los sistemas templados y tropicales, dijeron Darnajoux y Zhang. El umbral para la cantidad de molibdeno que un ecosistema necesita para activar o desactivar la fijación de nitrógeno de vanadio que encontraron en su estudio fue notablemente similar a los requisitos de molibdeno de fijación de nitrógeno encontrados para muestras que abarcan diversos biomas.
Los investigadores continuarán la búsqueda de la fijación de nitrógeno a base de vanadio en las latitudes del norte. También han dirigido sus ojos hacia áreas más cercanas al hogar, iniciando estudios de dinámica de micro y macronutrientes en bosques templados en Nueva Jersey, y planean expandir su trabajo a los sistemas tropicales.
Página Web de la Estación Experimental del Zaidín.
La enzima nitrogenasa o nitrogenasa que cataliza la reducción de N2 a amonio está constituida por dos metaloproteínas, la ferroproteína o nitrogenasa reductasa, y la ferromolibdoproteína o nitrogenasa. La primera es un homodímero (alpha:alpha). Y la segunda un tretámero (alpha:alpha:beta:beta) que contiene dos grupos P (P-clusters), uno, (8Fe-7S) y el otro, (Mo:7Fe-9S): homocitrato, que constituye el cofactor conocido como FeMoco (cofactor hierro molibdeno) a nivel del cual ocurre la reducción del N2 aunque se desconoce cómo y dónde se une el substrato y es activado. La Feproteína, activada por ATP-Mg, transfiere los electrones a la nitrogenasa que a su vez los distribuye entre N2 y protones para dar amonio e hidrógeno. Esta reducción de protones es siempre concomitante con la producción de amonio. Supone una pérdida de eficiencia del proceso por la parte correspondiente de energía que consume (un 25 por ciento). Algunas especies y cepas microbianas están provistas de una actividad hidrogenasa que recicla en parte la energía perdida por la liberación de hidrógeno. La enzima nitrogensa es fácilmente inactivada por oxígeno, de tal forma que todos los sistemas fijadores han desarrollado estrategias especiales para protegerse de concentraciones elevadas de este elemento y evitar su inactivación si es que se ha sintetizado, pues la expresión de los genes nif está estrictamente regulada, tanto por oxígeno como por nitrógeno combinado a través del sistema Ntr-NifA. Estas estrategias van desde la anaerobiosis total, como en Clostridium, a la producción de gran cantidad de polisacásridos extracelulares que hacen de filtro para el oxígeno, exclusión metabólica (Azotobacter) o la compartimentación, caso de las cianobacterias. En la simbiosis Rhizobium-leguminosa, la estructura del nódulo crea el ambiente microaerobio adecuado y la leghemoglobina facilita el transporte de oxígeno al bacteroide para soportar el metabolismo aerobio requerido para obtener la energía necesaria para la reducción del N2. Los requerimientos de la fijación por el molibdeno fue ya señalada en los años 30 por Bortels, pero recientemente se han descrito nitrogenasas alternativas en ausencia de molibdeno en el medio, que contienen otros elementos de transición, como vanadio o hierro denominadas a veces (nitrogenasas alternativas; nota de bloguero) . Una vez descifrada la química de la fijación se podría abrir la posibilidad de un proceso industrial alternativo al de Haber Bosch para la obtención de fertilizante nitrogenado. Sería interesante, pues el funcionamiento del sistema Haber Bosch, que produce unos 80 MTn. año de amonio, supone el 1 % del total de la energía consumida a nivel mundial. Para más información ver: http://www.rcsb.org/pdb/molecules/pdb26_1.html
